Менингит как осложнение после коронавируса
Случай из практики. Пациентка с менингитом COVID этиологии
Елена Владимировна заболела остро 7 мая, её беспокоили головная боль, тошнота, повторная рвота, высокая температура. 11 мая, несмотря на прием препаратов с обезболивающим эффектом, состояние больной ухудшилось, перестала вступать в контакт с родственниками. Бригадой скорой медицинской помощи Елена Владимировна доставлена в ИКБ №2, в отделение реанимации и интенсивной терапии. Из анамнеза было известно, что ее мама только что перенесла новую коронавирусную инфекцию.
В ОРИТ выполнен весь спектр необходимых исследований и проведен осмотр специалистами. Был диагностирован серозный менингоэнцефалит — воспаление головного мозга. Врачи ИКБ №2 предположили, что поражение головного мозга вирусной этиологии. Тяжесть состояния была обусловлена отеком мозга и интоксикацией. Учитывая прогрессирование явлений полиорганной недостаточности, больную перевели на искусственную вентиляцию легких.
Выполнены ПЦР исследования ликвора на все возможные агенты, вызывающие вирусный энцефалит – результаты отрицательные. В анализе крови отмечается высокий титр иммуноглобулинов на COVID-19. Заведующий отделением реанимации Владимир Борисович Ченцов предположил, что в данном случае, серозный менингоэнцефалит может быть вызван вирусом Sars-Cov-2.
Когда пришли результаты исследования на новую коронавирусную инфекцию — в ликворе методом ПЦР обнаружена РНК коронавируса COVID-19, подозрение врачей по поводу менингита коронавирусной этиологии подтвердились.
За время нахождения в ОРИТ Елена Владимировна получала всю необходимую терапию и уход, а, самое главное, наблюдалась профессионалами под руководством заведующего отделением Владимира Борисовича Ченцова. После стабилизации состояния пациентку перевели в 3 инфекционное отделение, где, благодаря лечению и внимательному отношению персонала с участием исполняющей обязанности заведующего отделением Анны Павловны Угриновой, пациентка выздоровела.
Елена Владимировна была одной из первых больных с менингитом COVID этиологии — уникальный случай мирового масштаба!
Несмотря на все сложности, включая тяжелое состояние больной и эксклюзивность случая, профессионалам ИКБ №2 удалось спасти этого замечательного человека, преподавателя по профессии.
Она улыбается, а мы улыбаемся вместе с ней!
Поражения нервной системы при COVID-19
До недавнего времени вопрос о том, поражает ли вирус SARS-CoV-2 структуры нервной системы, оставался открытым. С момента начала пандемии COVID-19 у заболевших отмечались отдельные неврологические симптомы, а с начала апреля в зарубежных источниках начали появляться отчеты о первых подтвержденных случаях поражения центральной нервной системы и периферических нервов. В данном материале мы приводим описания этих случаев. Отдельная благодарность за помощь в переводе описаний клинических случаев — Артуру Арсеньеву.
Предпосылки возможного инфицирования нервной системы
Некоторые специалисты предполагают, что SARS-CoV-2 не только воздействует на респираторный тракт, но и проникает в центральную нервную систему, вызывая неврологические расстройства. Механизмы возможного вовлечения центральной нервной системы различны, и авторы выделяют три наиболее вероятных варианта.
Во-первых, не исключается, что развитие дыхательной недостаточности, сопровождающей новую коронавирусную инфекцию, связано с вовлечением в патологический процесс не только нижних дыхательных путей, но и дыхательного центра в стволе головного мозга. Эпидемиологические исследования показывают, что при развитии коронавирусной инфекции среднее время от появления первых симптомов до развития дыхательной недостаточности составляет 5 дней. За это время вирус может проникнуть через гематоэнцефалический барьер через кровь или транссинаптическим путем и воздействовать на нейроны ствола головного мозга, нарушив тем самым работу дыхательного центра.
Во-вторых, нейроинвазивный потенциал COVID-19 исследуется на примере близких к нему по строению коронавирусов. SARS-CoV-1 обнаруживался в головном мозге пациентов и экспериментальных животных — значит, не исключено, что проникновение в ЦНС возможно и для SARS-CoV-2. Для инвазии в клетки COVID-19 использует ангиотензинпревращающий фермент 2 типа (АПФ2) в качестве рецептора, который обнаруживается на поверхности нейронов и глиальных клеток в головном мозге. Взаимодействие коронавируса с этими рецепторами может приводить к прямому повреждению нейронов без развития воспаления. Аналогичная картина была продемонстрирована в серии клинических случаев заражения SARS-CoV-1.
Рассматриваются и другие механизмы поражения нервной системы при новой коронавирусной инфекции. Особое внимание уделяется иммунным механизмам, не исключается вероятность аутоиммунных воздействий. Развитие цитокинового шторма при коронавирусной инфекции повышает проницаемость гематоэнцефалического барьера, делая возможным бесконтрольное проникновение вирусов, бактерий, иммунных клеток, токсичных метаболитов и воспалительных агентов в структуры ЦНС. Воздействие этих факторов на ткань головного мозга и его оболочки может привести к развитию неврологических симптомов без непосредственного проникновения SARS-CoV2, однако данные состояния все равно можно считать ассоциированными с этой инфекцией.
Источники:
Неврологические симптомы у пациентов с COVID-19
В актуальных исследованиях показано, что около 8 % пациентов с подтвержденной инфекцией COVID-19 жаловались на головную боль, 1 % — на тошноту и рвоту. Исследование 214 пациентов подтверждает, что 88 % больных в тяжелом состоянии (78 из 88 в исследуемой группе) демонстрируют такие неврологические симптомы, как острые цереброваскулярные состояния и нарушения сознания. По данным этого же исследования, у некоторых пациентов характерные симптомы коронавирусной инфекции появляются лишь спустя некоторое время после развития первых неврологических проявлений. По данным патологоанатомических исследований, у пациентов, умерших от последствий инфекции COVID-19, были выявлены признаки отека мозга.
Таким образом, специалисты сферы здравоохранения, работающие с COVID-19, должны быть насторожены в отношении возможного нейроинвазивного потенциала вируса. Далее будет описано несколько случаев поражения нервной системы у больных с COVID-19.
Источники:
Острая некротизирующая геморрагическая энцефалопатия
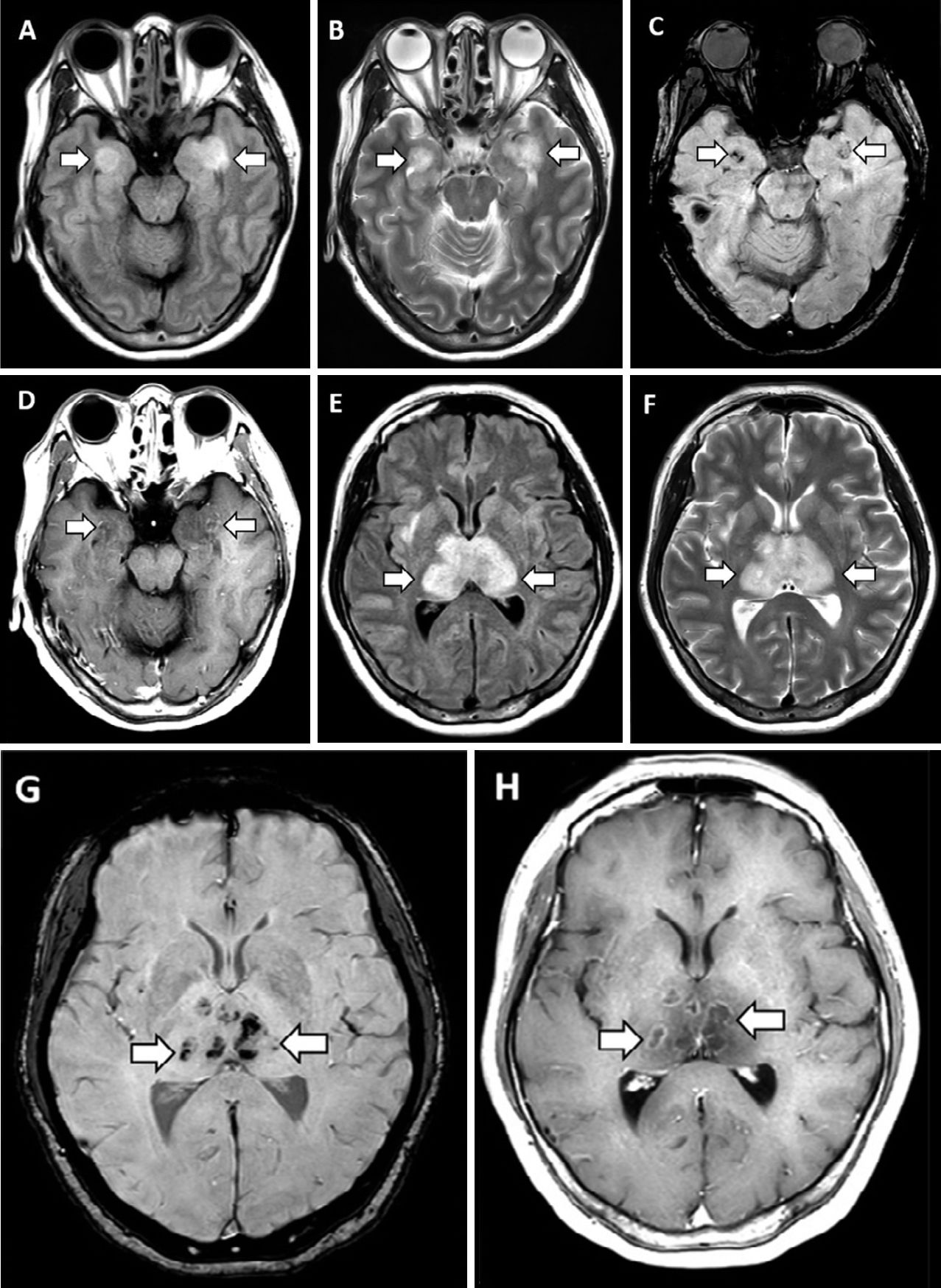
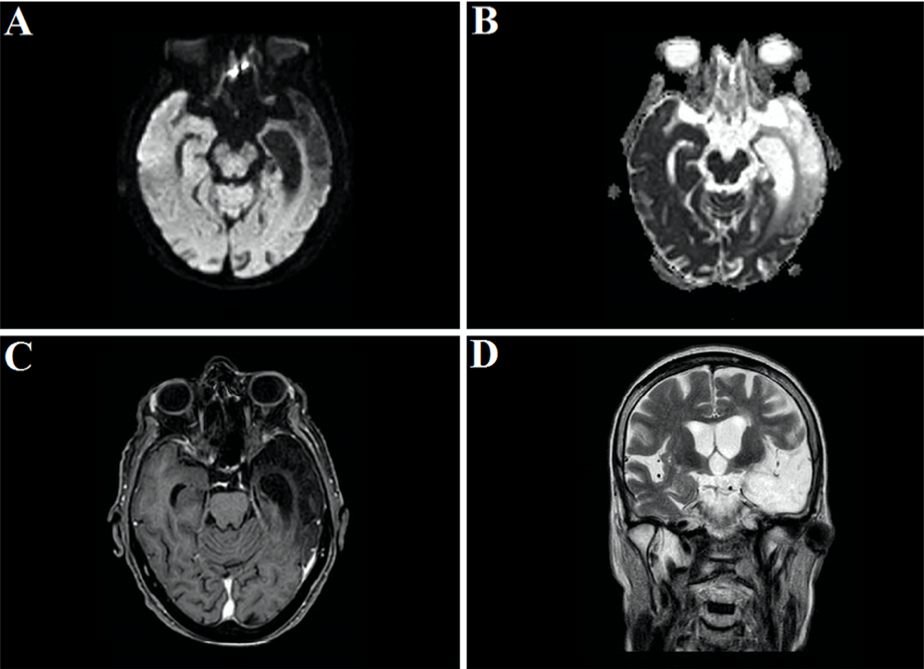
31 марта в журнале Radiology был описан случай COVID-19-ассоциированной острой некротизирующей геморрагической энцефалопатии. Данное состояние встречается редко и может быть ассоциировано с вирусными инфекциями, однако его связь с COVID-19 была установлена впервые. Первой пациенткой, демонстрирующей развитие энцефалопатии, стала женщина около шестидесяти лет с жалобами на кашель, лихорадку и помутнение сознания в течение трех дней. Диагноз новой коронавирусной инфекции был подтвержден методом ПЦР при исследовании мазка из полости носа. В цереброспинальной жидкости не было обнаружено ни бактериального роста, ни наличия вирусов простого герпеса 1 и 2 типов, вируса ветряной оспы и возбудителя лихорадки Западного Нила. Провести исследование цереброспинальной жидкости на предмет наличия SARS-CoV-2 не удалось. Компьютерная томография головы без введения контраста показала наличие симметричных участков просветления в медиальных отделах таламуса, а также нормальные данные ангиографии и венографии. На МРТ головного мозга были заметны участки усиления сигнала в таламусе, медиальных отделах височных долей и субинсулярных областях, свидетельствующие о геморрагии.
.
Полученные данные инструментальных исследований свидетельствуют о наличии острой некротизирующей энцефалопатии. Это редкое осложнение вирусных инфекций связано с развитием цитокинового шторма, который приводит к нарушению целостности гематоэнцефалического барьера. При этом не наблюдается инвазии вируса в головной мозг или демиелинизации. Данное состояние чаще описывают в педиатрической практике, но не исключено его развитие и у взрослых.
Источники:
Менингит и энцефалит
Позже в International Journal of Infectious Diseases был описан первый случай менингита и энцефалита, ассоциированных с COVID-19. Пациент 24 лет в конце февраля обратился к врачу с жалобами на слабость, головную боль и лихорадку. Врач предположил развитие гриппа и назначил ланинамивир и антипиретики. На пятый день заболевания пациент обратился в другую клинику в связи с ухудшением состояния, прошел рентгеновское исследование грудной клетки и анализ крови на наличие коронавирусной инфекции, анализ крови оказался отрицательным. На девятый день заболевания мужчина был найден в собственном доме в бессознательном состоянии, лежащим в собственных рвотных массах. По пути в стационар у пациента развились генерализованные судороги, продолжавшиеся одну минуту. Была заметна отечность в области шеи. По прибытию в стационар нарушение сознания пациента было оценено в 6 баллов по шкале комы Глазго (E4 V1 M1) с гемодинамической стабильностью. Анализ крови показал нейтрофильный лейкоцитоз с лимфопенией, высокий уровень С-реактивного белка. В бесцветной, прозрачной цереброспинальной жидкости были обнаружены мононуклеары и полиморфонуклеарные клетки, а методом ПЦР было выявлено наличие РНК SARS-CoV-2, анализ мазка из носоглотки при этом был отрицательным. В сыворотке крови не были обнаружены антитела типа IgM против вируса простого герпеса 1 типа и вируса ветряной оспы. Системная КТ не выявила отека мозга. КТ органов грудной клетки показала участки «матового стекла» в правой верхней доле и в обеих нижних долях. МРТ головного мозга показала гиперинтенсивные участки по стенке правого бокового желудочка и изменения сигнала в правой медиальной височной доле и гиппокампе, что предполагает возможность развития COVID-19-ассоциированного менингита и энцефалита.
.
В связи с обнаружением COVID-19 в цереброспинальной жидкости в данном случае можно говорить как о повышении проницаемости гематоэнцефалического барьера, так и о нейроинвазивном потенциале возбудителя коронавирусной инфекции.
Источники:
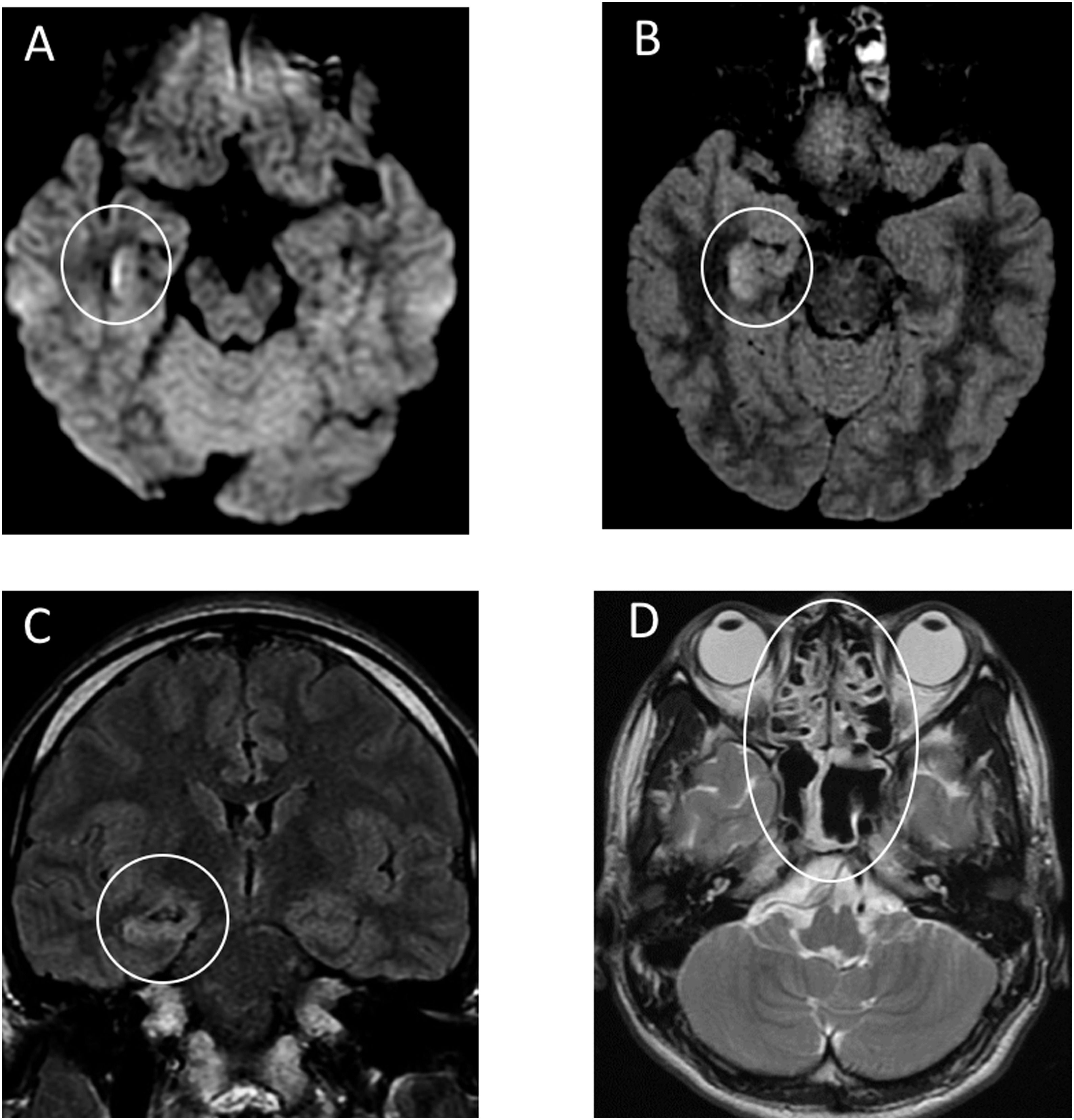
Поражение обонятельных луковиц
Одним из характерных клинических симптомов новой коронавирусной инфекции является аносмия, иногда — в сочетании с гипогевзией. Причиной развития аносмии в случае вирусной инфекции принято считать застойные явления в слизистой оболочке полости носа, ведущие к обструкции носовых ходов и временной потере чувствительности. Однако у некоторых пациентов аносмия становится перманентной, что может быть связано с необратимым вирусным повреждением нейронов. Важно отметить, что АПФ2 — рецепторы, необходимые для инвазии SARS-CoV-2, — экспрессируются в обонятельном эпителии.
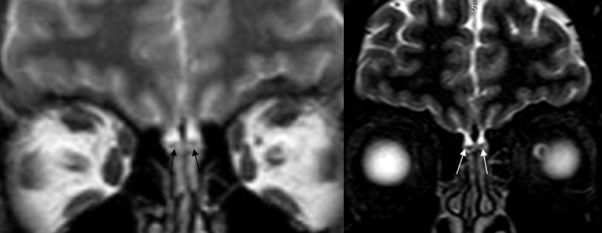
Особенности строения обонятельных областей исследуют методом МРТ. Основные находки на МРТ при аносмии, вторичной по отношению к инфекциям верхних дыхательных путей, — это снижение уровня сигнала, что говорит об уменьшении плотности нейронов, которая коррелирует с обонятельной функцией.
13 апреля в журнале Academic Radiology был представлен случай изолированной аносмии у пациента с новой коронавирусной инфекцией, подтвержденной методом ПЦР. Сообщается, что на МРТ обонятельных областей данного пациента интенсивность сигнала была нормальной, отсутствовали признаки застоя. Это говорит об отсутствии анатомических изменений, которые мог бы вызывать вирус SARS-CoV-2, а значит, нарушения обоняния обусловлены скорее функциональными изменениями, связанными с действием вируса.
.
Для получения более подробных данных об этих изменениях авторами было предложено проводить комбинированные исследования, например, сочетание однофотонной эмиссионной компьютерной томографии с МРТ.
Источники:
Синдром Гийена-Барре
1 апреля в журнале Lancet был описан первый случай синдрома Гийена-Барре, ассоциированного с COVID-19. В конце февраля 61-летняя женщина обратилась к врачу с жалобами на остро возникшую слабость в обеих ногах. Она вернулась из Уханя в конце января, но отрицала развитие у нее таких симптомов, как лихорадка, кашель, боль в груди и диарея. Функциональные показатели работы ее дыхательной системы были в норме, аускультация легких не выявила признаков патологии. Неврологическое исследование показало симметричную слабость (4/5 по шкале оценки мышечной силы MRC) и арефлексию в нижних конечностях. Симптомы прогрессировали: через три дня сила мышц составляла 4/5 для рук и 3/5 для ног. В дистальных отделах конечностей начала снижаться чувствительность к прикосновениям и уколам иглой. Исследование цереброспинальной жидкости на четвертый день после обращения показало нормальное количество клеточных элементов и высокий уровень белка. Проведенная на пятый день ЭНМГ показала задержку проводимости в дистальных отделах верхних и нижних конечностей и отсутствие F-волн, что свидетельствовало о наличии демиелинизирующей нейропатии. Женщине был поставлен диагноз: синдром Гийена-Барре.
На восьмой день у пациентки развились сухой кашель и лихорадка. КТ органов грудной клетки показала участки «матового стекла» в обоих легких. В мазках слизи из полости носа методом ПЦР была обнаружена РНК SARS-CoV-2. После проведенного курса лечения лопинавиром и ритонавиром состояние пациентки улучшилось. На 30 день с момента обращения восстановилась нормальная мышечная сила в руках и ногах, появились сухожильные рефлексы. У родственников, контактировавших с больной новой коронавирусной инфекцией, неврологических симптомов отмечено не было.
Авторы предполагают, что за развитие синдрома Гийена-Барре у данной пациентки ответственен именно COVID-19. Это вносит в перечень возможных механизмов поражений нервной системы еще один — аутоиммунные воздействия при инфицировании новым коронавирусом.
Таким образом, на данный момент в литературе уже были представлены случаи поражения структур нервной системы при инфицировании COVID-19 по трем основным механизмам: цитокиновый шторм, прямое повреждающее действие и аутоиммунное воздействие. Публикации новых клинических случаев позволят пролить свет на особенности этих механизмов. Уже сейчас становится ясно, что каждый специалист, работающий с COVID-19, должен быть насторожен в отношении возможного развития неврологических симптомов и вовремя их диагностировать.
Источники:
Потеря контроля над течением эпилепсии
Развитие эпилепсии в этом случае не совсем верно считать ассоциированным с COVID-19 — пациентка имела постэнцефалитическую эпилепсию после другого вирусного заболевания и успешно контролировала возникновение эпилептических припадков в течение двух лет. Однако изменение течения заболевания после инфицирования коронавирусом заставляет задуматься о возможном влиянии новой вирусной инфекции на течение контролируемой эпилепсии.
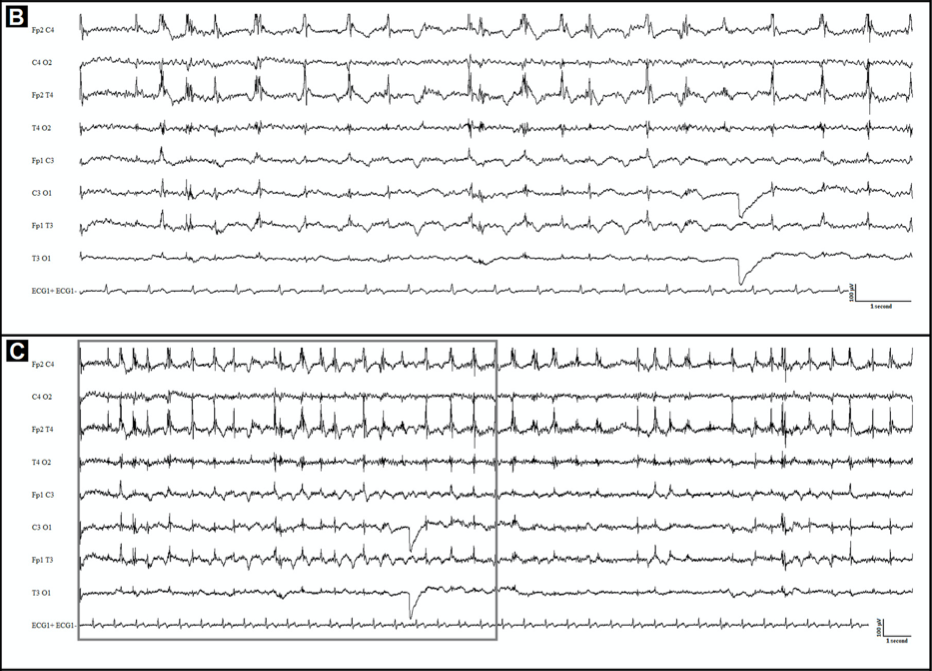
78-летняя женщина поступила в отделение неотложной помощи с продолжающимися миоклоническими судорогами правой половины лица и тела. В анамнезе — артериальная гипертензия и постэнцефалитическая эпилепсия. В возрасте 76 лет женщина перенесла герпесвирусный энцефалит, который манифестировал с повторяющихся оральных автоматизмов и афазии в течение 6 часов. На ЭЭГ наблюдались перемежающиеся эпилептиформные разряды над левой височной долей, формирующие бессудорожный эпилептический статус. Эпистатус был успешно купирован, после чего сохранялась слабо выраженная афазия и небольшая слабость конечностей. С целью профилактики приступов пациентка принимала вальпроевую кислоту и леветирацетам, ввиду чего эпилептические приступы не проявляли себя в течение двух лет.
Утром 12 марта 2020 года у пациентки развился фокальный эпилептический статус без продромальных симптомов. Температура на момент госпитализации составляла 36,1 °C. Неврологический осмотр выявил легкую афазию, паралич правой половины лица, пронацию правой руки и спастическое отведение правой ноги. Пациентка демонстрировала продолжающиеся миоклонические судороги век правого глаза и верхней губы в течение двух часов. Терапия проводилась при помощи вальпроевой кислоты и мидазолама внутривенно. На ЭЭГ фиксировалась нерегулярная, высокоамплитудная дельта-активность, в основном локализованная в лобно-центрально-височной области слева.
.
Противоэпилептическая терапия привела к регрессу эпистатуса. КТ головного мозга не выявила острой патологии, на МРТ головного мозга описывались очаги глиоза и атрофии височной и теменной долей слева, отсутствие новых патологических изменений и накоплений контрастного вещества. Рентген грудной клетки — без особенностей. Из лабораторных данных обращают на себя внимание лимфоцитопения и тромбоцитопения.
.
12 часов спустя у пациентки развилась лихорадка без типичных для коронавирусной инфекции респираторных проявлений. Сатурация была в норме. Анализ крови демонстрировал дальнейшее снижение уровней лейкоцитов и тромбоцитов. C-реактивный белок находился на уровне 29,7 мг/л, прокальцитонин — 0,07 нг/мл. Начатая антибактериальная терапия не оказала влияния на лихорадку. Исследования крови и мочи не выявили наличия бактерий, грибов или нейротропных вирусов.
Из эпидемиологического анамнеза стало известно, что на предыдущей неделе пациентка виделась со своим сыном, который контактировал с людьми, позитивными по COVID-19, и до этого находился на превентивной изоляции. ПЦР мазков из носо- и ротоглотки выявила у женщины наличие COVID-19. Пациентка была переведена в инфекционное отделение, получала терапию по схеме лопинавир-ритонавир + гидроксихлорохин с положительным эффектом. Дальнейшие исследования легких не выявили интерстициальной пневмонии. Пациентка не получала оксигенотерапию, судорожные приступы не рецидивировали. 28 марта была выписана после двух отрицательных ПЦР мазков при отсутствии лихорадки.
В данном случае коронавирус, возможно, стал триггером к активации эпилептической активности у пациентки, перенесшей ранее постэнцефалитическую эпилепсию. Нужно отметить, что инвазию вируса в ЦНС установить не удалось, так как не были проведены спинномозговая пункция и ПЦР цереброспинальной жидкости. Пока что можно предполагать, что коронавирусная инфекция может являться тем триггером, который в отсутствие других симптомов может приводить к рецидивам некоторых заболеваний ЦНС.
Источники:
Неврологическая манифестация COVID-19
Подводя итог, приводим инфографику с наглядным изображением частоты распространения основных неврологических симптомов, которые отмечались у пациентов с COVID-19 по всему миру.
.
Менингит: многоликий убийца
Менингит: многоликий убийца
Менингит — опаснейшее заболевание, часто приводящее к инвалидности или смерти. Рисунок в полном размере можно посмотреть по ссылке.
Автор
Редакторы
Все знают, что менингит — очень опасная болезнь, но, тем не менее, часто возникает вопрос, стоит ли вакцинироваться от нее, ведь она не так уж и распространена в наших широтах. В этой статье спецпроекта «Вакцинация» мы рассказываем, какими патогенами может вызываться менингит, что делать, если вы подозреваете, что заболели, и каким образом максимально обезопасить себя от этой болезни и избежать ужасных последствий.
Вакцинация
Генеральный партнер спецпроекта — Zimin Foundation.
Изобретение вакцин кардинально изменило жизнь человечества. Многие болезни, уносившие тысячи, а то и миллионы жизней ежегодно, теперь практически не встречаются. В этом спецпроекте мы не только рассказываем об истории возникновения вакцин, общих принципах их разработки и роли вакцинопрофилактики в современном здравоохранении (этому посвящены первые три статьи), но и подробно говорим о каждой вакцине, включенной в Национальный календарь прививок, а также вакцинах против гриппа и вируса папилломы человека. Вы узнаете о том, что собой представляет каждый из возбудителей болезней, какие существуют варианты вакцин и чем они различаются между собой, затронем тему поствакцинальных осложнений и эффективности вакцин.
Для соблюдения объективности мы пригласили стать кураторами спецпроекта Александра Соломоновича Апта — доктора биологических наук, профессора МГУ, заведующего лабораторией иммуногенетики Института туберкулеза (Москва), — Сусанну Михайловну Харит — доктора медицинских наук, профессора, руководителя отдела профилактики НИИ детских инфекций (Санкт-Петербург), — а также Сергея Александровича Бутрия — педиатра, автора блога «Заметки детского врача».
Менингит — заразное заболевание, которое может развиться как самостоятельно, так и вследствие других болезней (например, иммунодефицитов, повреждений черепа, общего сепсиса). Свое название болезнь берет от латинского слова meningis, что означает «мозговая оболочка». В медицине под термином «менингит» врачи обычно подразумевают воспаление только мягкой оболочки мозга. Менингит может быть вызван огромным количеством патогенов: вирусами, бактериями и даже простейшими.
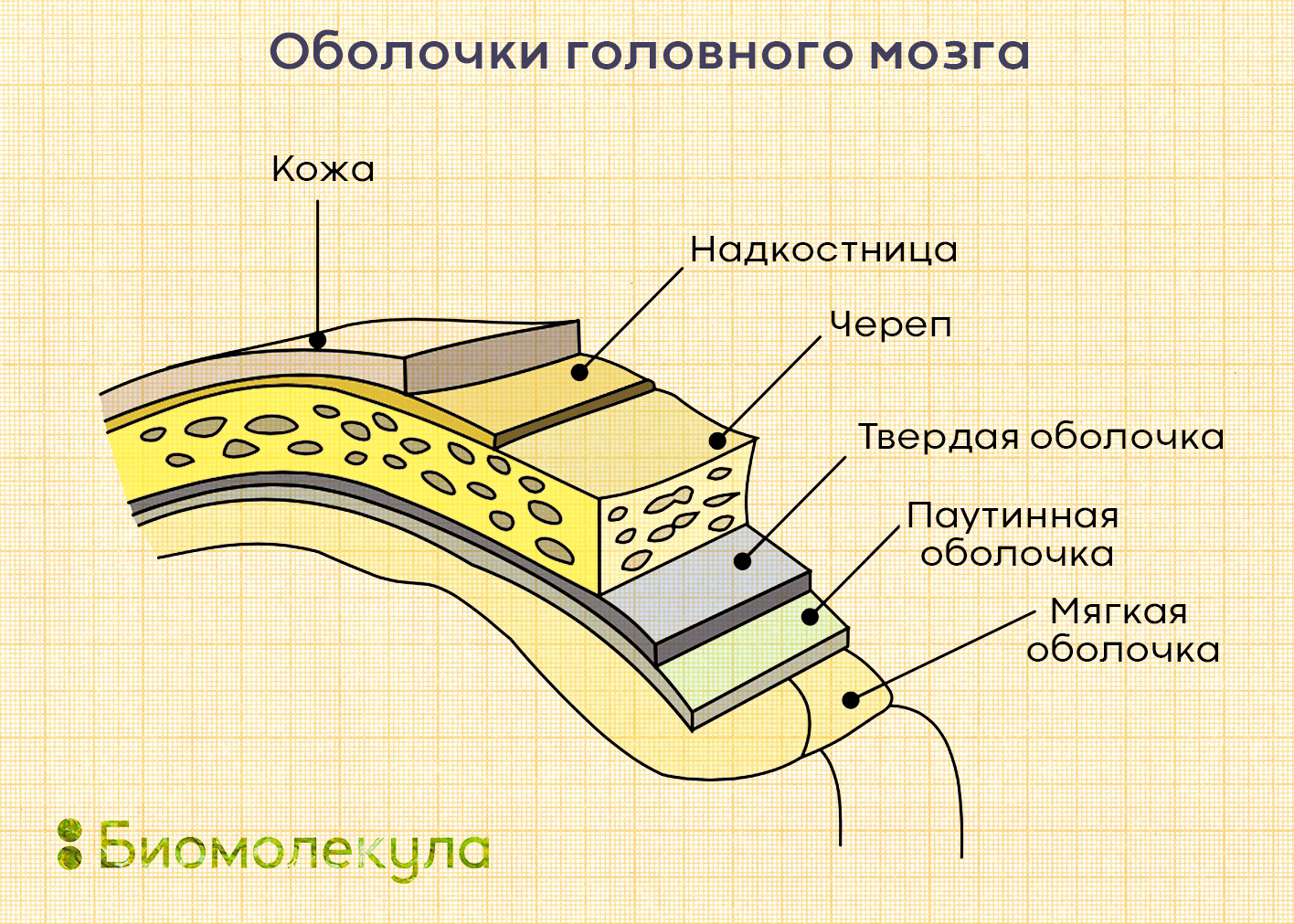
Оболочки головного мозга
Мозговая оболочка покрывает наш головной и спинной мозг и состоит из трех слоев: твердой оболочки, паутинной и мягкой (рис. 1). Твердая находится ближе всего к поверхности. Она состоит из соединительной ткани и срастается с надкостницей костей основания черепа и швами свода черепа. Паутинная оболочка находится под твердой и имеет вид тонкой паутины, состоящей из соединительной ткани. Кроме того, она содержит большое количество фибробластов и глиальные клетки. Мягкая оболочка находится ближе всего к мозгу, плотно к нему прилегая и повторяя все его борозды. Состоит из рыхлой соединительной ткани, пронизанной питающими мозг сосудами.
Рисунок 1. Оболочки головного мозга
Менингит может иметь серьезные последствия. «Когда дело касается менингита, то, чего ты не знаешь, может сильно тебе навредить», — пишет Джейми Шанбаум, американская параатлетка, которая перенесла менингококковый менингит в юности. Из-за менингококковой инфекции, самого известного возбудителя менингита, ей пришлось ампутировать ноги ниже колена, тем не менее она нашла в себе силы принять это и достигла успехов в велосипедном спорте.
Менингит сквозь века
История менингита начинается еще в древности (рис. 2) [1]. На протяжении столетий врачи и ученые исследовали эту болезнь и пытались изобрести способы ее лечения и диагностики. Очень важные открытия были совершены в XVIII и XIX веках, когда сначала Гаспар Вассо, Андре Мэтти, Элиза Норс описали патогенез эпидемического менингита, а затем Генрих Квинке применил и описал технику люмбальной пункции для ранней диагностики менингита, что позволило значительно продвинуться в сторону успешной борьбы с ним.
Рисунок 2. История менингита. Первые описания вспышек менингита: II в. до н.э. — Аретей, I в н.э. — Цельс, VII в. — Павел Эгинский. 1661 год. Британский ученый-медик Томас Уиллис впервые описал у пациентов «воспаление мозговых оболочек с постоянной лихорадкой». XVIII век. Шотландский врач Роберт Уайт сделал классическое описание туберкулезного менингита и его стадий, а Гаспар Вассо, Андре Мэтти, Элиза Норс описали патогенез эпидемического (менингококкового) менингита. XVIII–XIX века. Бактериолог Георг Йохманн из Германии и врач Саймон Флекснер из Америки впервые успешно применили терапию сывороткой крови иммунизированной против менингита лошади для лечения менингококкового менингита. 1891 год. Немецкий хирург Генрих Квинке впервые применил и описал технику люмбальной пункции спинномозговой жидкости для ранней диагностики менингита. XIX век. Определен спектр патогенов, вызывающих менингит, включая Streptococcus pneumoniae, Neisseria meningitidis и Haemophilus influenzae. XX век. Разработана терапия менингита антибиотиками, а также первая вакцина против бактериального менингита, вызванного патогенами Neisseria meningitidis и Haemophilus influenzae.
Кто вызывает менингит?
Бактериальный менингит
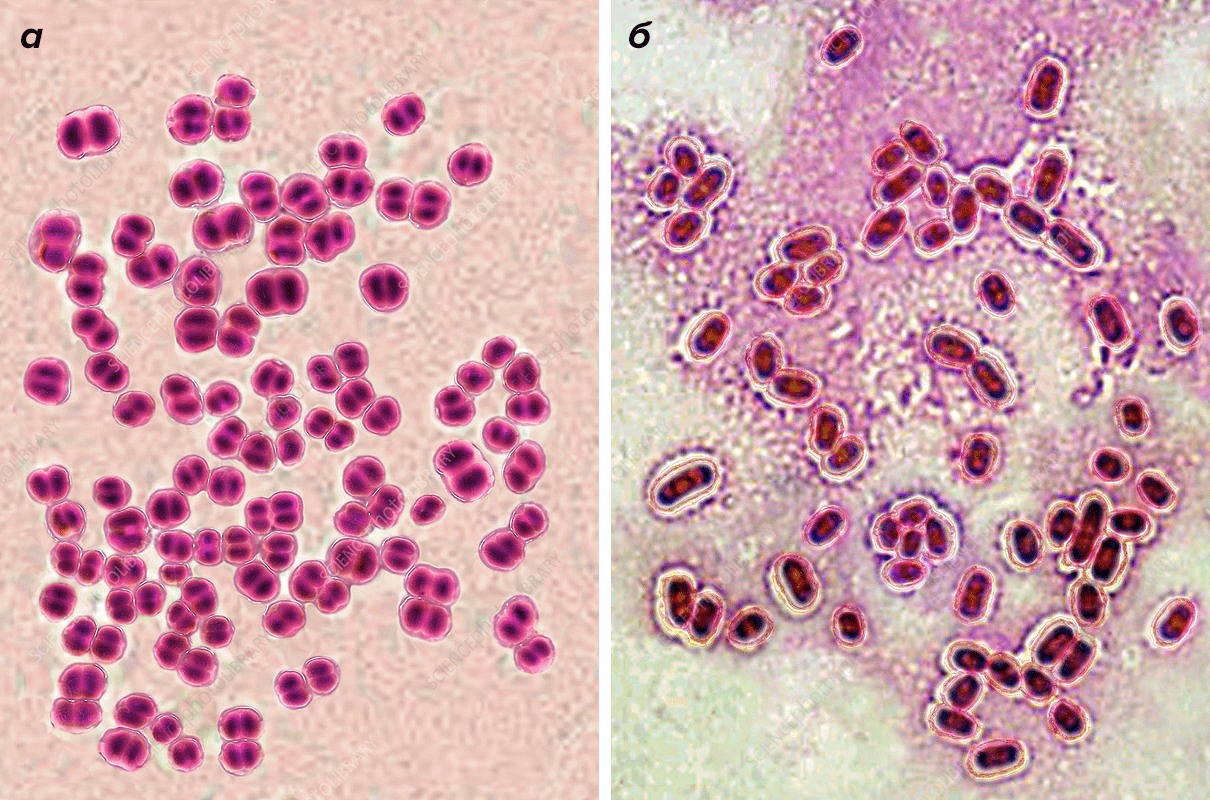
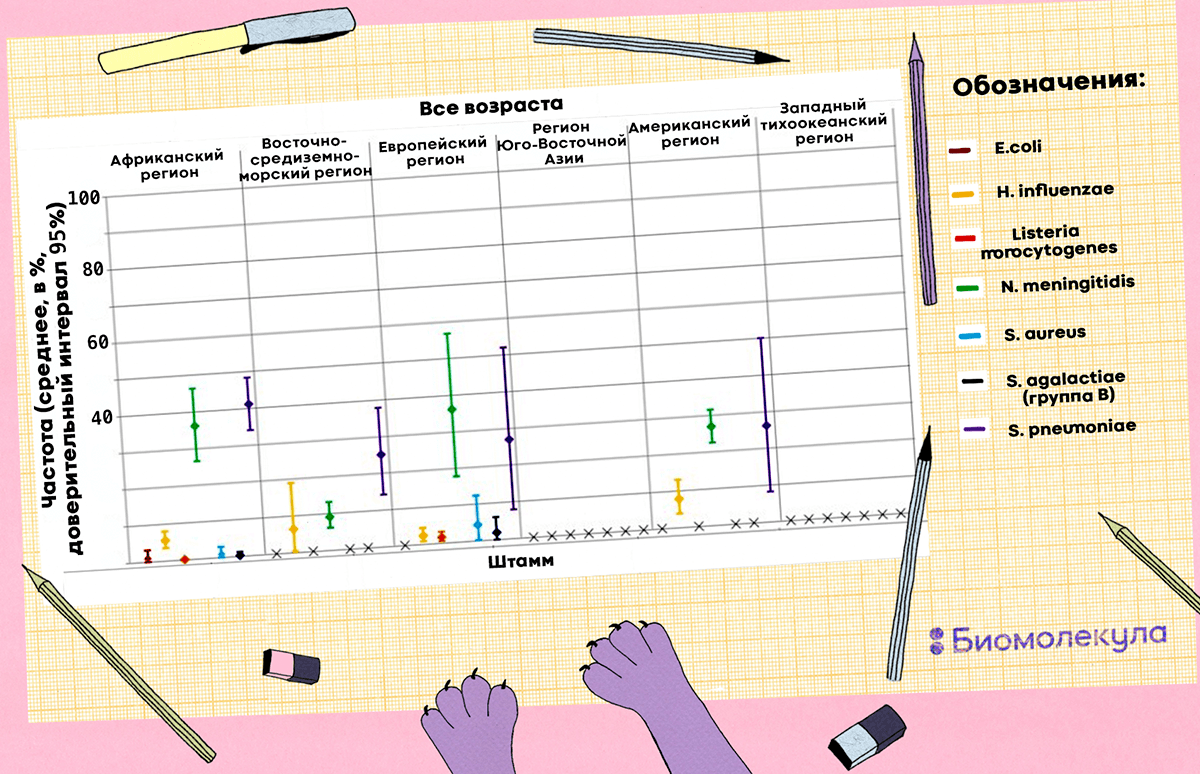
Наиболее распространенные патогены, вызывающие бактериальный менингит, — это бактерии Neisseria meningitidis и Streptococcus pneumoniae (рис. 3). Для разных регионов их встречаемость относительно всех случаев бактериального менингита варьирует в пределах 9–35% и 25–40% соответственно [2]. Кроме них в патогенезе бактериального менингита могут принимать участие Haemophilus influenzae, Escherichia coli, Listeria monocytogenes, Staphylococcus aureus, Streptococcus agalactiae (рис. 4).
Рисунок 3. Основные бактериальные возбудители менингита: а — Neisseria meningitidis; б — Streptococcus pneumoniae
Рисунок 4. Частота встречаемости семи бактериальных патогенов, вызывающих менингит, относительно случаев заболевания по географическим регионам
В целом в мире ситуация по заболеваемости бактериальным менингитом неутешительная. Общее число случаев заболевания увеличилось с 2,5 до 2,8 миллионов за 26 лет (с 1990 по 2016 годы) [3]. Чаще всего эпидемии возникают из-за распространения бактерии N. meningitides [4]. Однако если посмотреть на заболеваемость не во время вспышек, а в «мирное» время, то чаще всего болезнь вызывает S. pneumoniae, а не N. meningitidis. Общую картину динамики заболеваемости на примере США можно отследить по графику на рисунке 5.
Рисунок 5. Заболеваемость менингитом, вызванным различными бактериями, с 1997 до 2010 года в США
В 1887 году Антон Вейксельбаум обнаружил бактерию Neisseria meningitidis (менингококк) в спинномозговой жидкости пациента с менингитом и предположил, что именно она является причиной болезни [5]. Так и оказалось. Под микроскопом бактериальные клетки располагаются попарно и окружены капсулой. Менингококк подразделяют на тринадцать серогрупп [6], шесть из которых вызывают опасное для человека заболевание. Это серогруппы A, B, C, W-135, X и Y. Смертность при менингококковой инфекции велика, она составляет 8–15% от числа заболевших. При этом выделяют две формы менингококковой инфекции: менингит и менингококковый сепсис (менингококцемию), причем последняя намного более опасна.
Формы менингококковой инфекции
Менингококковая инфекция может вызывать как менингит (около 50% случаев), так и менингококковый сепсис (35–40% случаев) а иногда и оба этих заболевания одновременно [7]. В остальных 10% случаев развиваются очаговые заболевания, например, пневмония или артрит. Менингококковый сепсис часто является причиной полиорганной недостаточности, поэтому смертность от него чрезвычайно велика (около 40%), а у 20% выживших наблюдаются серьезные неврологические нарушения, проблемы со слухом и зрением, а также частичная или полная ампутация конечностей.
В СМИ с завидной частотой появляются сообщения о гибели детей от менингококцемии. В 2019 году случилась трагедия — в Екатеринбурге от менингита скончался маленький мальчик. С момента повышения температуры до комы и смерти прошли всего одни сутки. В 2018 году по дороге из Петербурга в Москву плохо себя почувствовала девочка. Мать подозревала у нее ангину, а медики, осмотревшие ее в Твери, посоветовали доехать до Москвы. Когда уже в Москве был выявлен менингит, спасти ребенка не удалось.
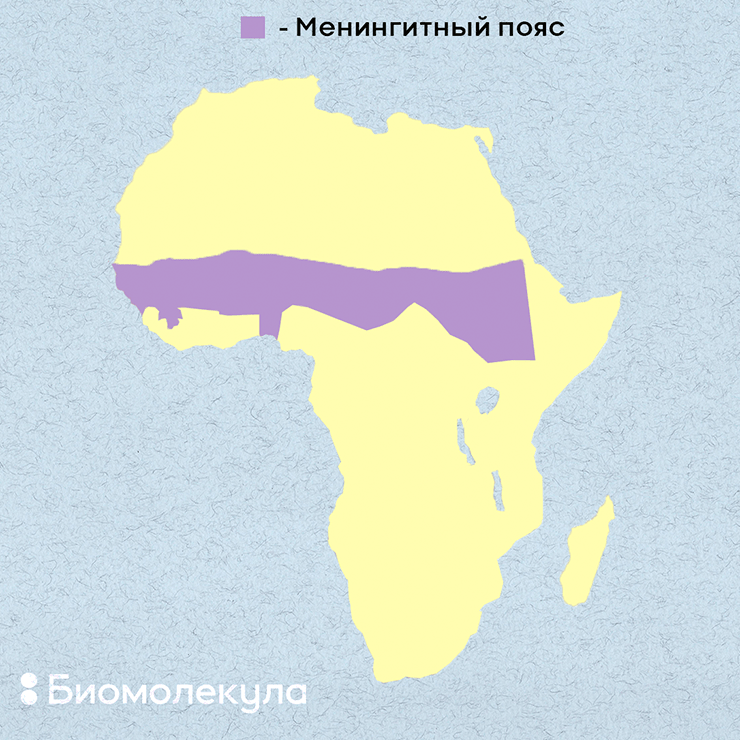
Рисунок 6. «Менингитный пояс» в Африке. В него попадают Сенегал, Мали, Буркина-Фасо, Нигерия, Нигер, Чад, Судан и другие страны.
Менингококковый менингит особенно распространен в Африке к югу от Сахары — в так называемом «менингитном поясе» (рис. 6), включающем 26 стран от Сенегала на западе до Эфиопии на востоке. Этому способствуют стесненные жилищные условия, антисанитария, неблагоприятные погодные условия. Так, пыль, поднимаемая там ветром в сухой сезон (с декабря по июнь), может вызывать повреждения слизистой носоглотки, создавая благоприятную почву для развития патогенных бактерий.
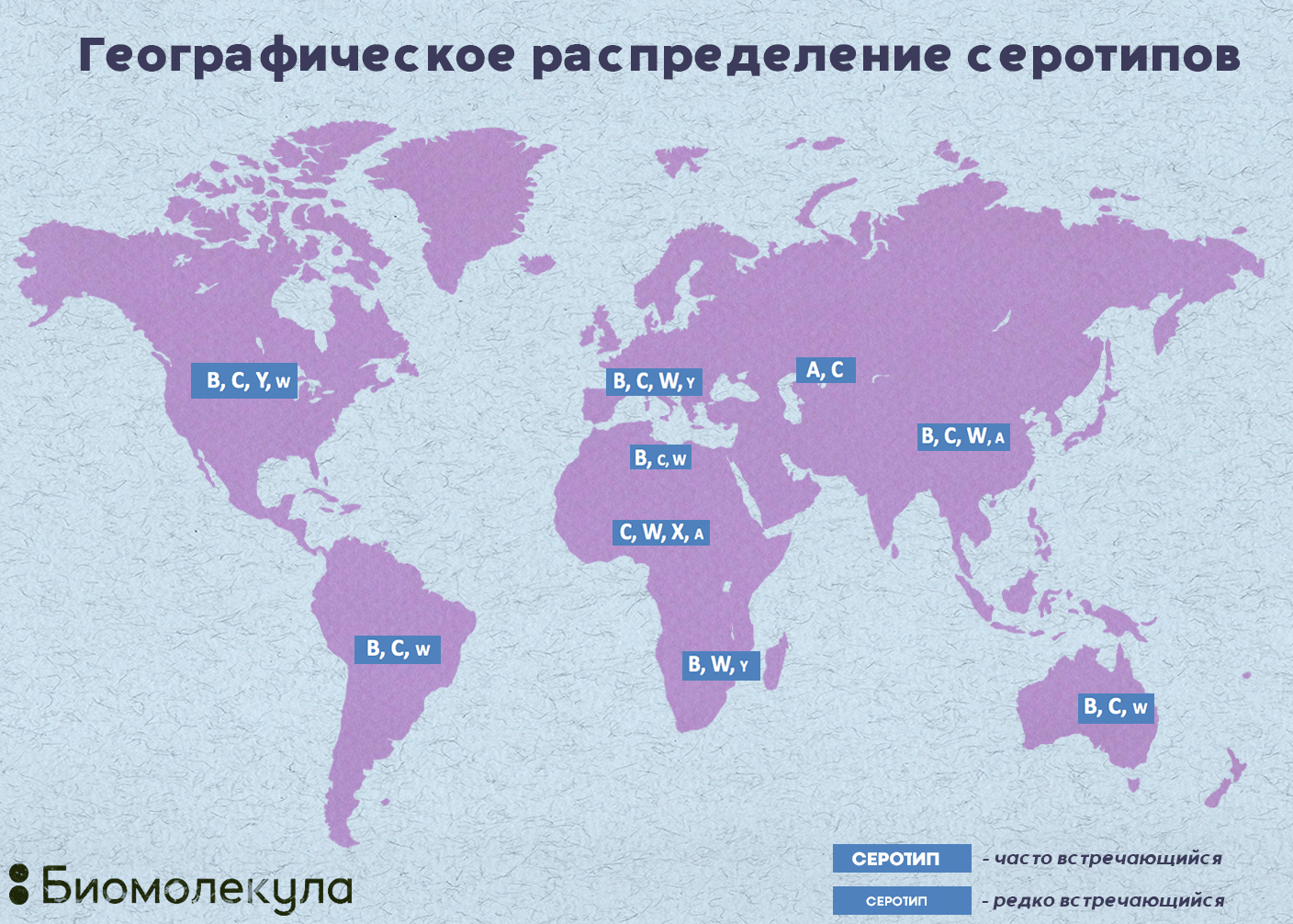
Распространение различных серогрупп менингококка различается в разных регионах. Например, в Европе преобладают серотипы В и С, в Африке — А, W-135, C, X (рис. 7).
Рисунок 7. Географическое распределение серотипов Neisseria meningitidis. На территории России в эпидемический процесс вовлечены N. meningitidis серогрупп А, В и С, данные о распространенности других серогрупп немногочисленны [8].
Практически каждый год в Африке случается эпидемия менингококкового менингита, при которой заболевает от 25 до 200 тысяч человек [9]. За последние 30 лет случилось две крупные эпидемии. В 1996 году в странах менингитного пояса заболело около 100 000 человек, из которых 10 000 погибло. Не так давно, в 2009 году, произошла еще одна эпидемия. По данным ВОЗ, с января по март погибло более 1100 жителей Нигерии, Нигера, Буркина-Фасо и Мали, а заразились более 13 000. Сильнее всего пострадала Нигерия — 562 летальных случая и около 9000 заболевших. За первые месяцы 2020 года в Африке уже было зарегистрировано 1784 случая менингококкового менингита со смертностью 5%. Снизить опасность эпидемии может помочь своевременная и качественная вакцинация.
В России менингококковый менингит встречается не так часто, как в Африке и даже в Европе. На это влияет в том числе холодный климат, в котором возбудители не так активно распространяются. Однако и в нашей стране случаи заболевания выявляются регулярно, например, серотипы менингококка А и С вызывают около 54% случаев болезни.
По данным Роспотребнадзора, в настоящее время в России заболеваемость менингококковым менингитом растет, хотя ранее было отмечено многолетнее снижение. За два года, с 2016-го по 2018-й, она увеличилась на 40%. Это в том числе связано с тем, что вспышки заражения менингитом имеют некоторую цикличность, свойственную эпидемическому процессу. Частота менингококковой инфекции в 2018 году составила 0,7 человек на 100 тыс. населения.
Streptococcus pneumoniae, он же пневмококк, — бактерия семейства стрептококков [10]. Всего существует около 90 серотипов этой бактерии, однако более 70% заболеваний вызывают серотипы 6–11. Опасна эта бактерия не только тем, что она может вызвать менингит. На ее счету такие заболевания, как пневмония, синусит, заражение крови и ушные инфекции. Она является самой распространенной причиной менингита у детей старше 5 лет и у взрослых [11]. Опасаться этой бактерии точно стоит не меньше, чем менингококка. Она встречается во всем мире, однако чаще всего пневмококковый менингит поражает людей в Африке [12]. В России примерно 25% бактериальных менингитов приходится на пневмококковую инфекцию [13].
До введения вакцинации гемофильная палочка Haemophilus influenzae типа В (так называемый ХИБ), в норме обитающая в носоглотке, была самой частой причиной бактериального менингита у детей до 5 лет [14]. ХИБ распространена повсеместно, в России около 10% случаев бактериальных менингитов вызваны именно этим патогеном [15]. Около 5% заболевших менингитом, вызванным ХИБ, погибает даже в случае своевременного лечения антибактериальными препаратами (в группе с тяжелым течением — до 30%), а у трети выздоровевших наблюдаются серьезные нарушения слуха и другие неврологические осложнения на всю оставшуюся жизнь.
Туберкулезный менингит
Несколько особняком стоит менингит, развивающийся в результате заражения туберкулезом. Туберкулезный менингит практически никогда не возникает сам по себе, а появляется как вторичная патология при поражении органов бактерией Mycobacterium tuberculosis, или палочкой Коха (рис. 8) [16], [17], когда те распространяются из первичного очага по всему организму по кровеносным сосудам [17].
Рисунок 8. Бактерия Mycobacterium tuberculosis
BSIP/UIG, Getty Images
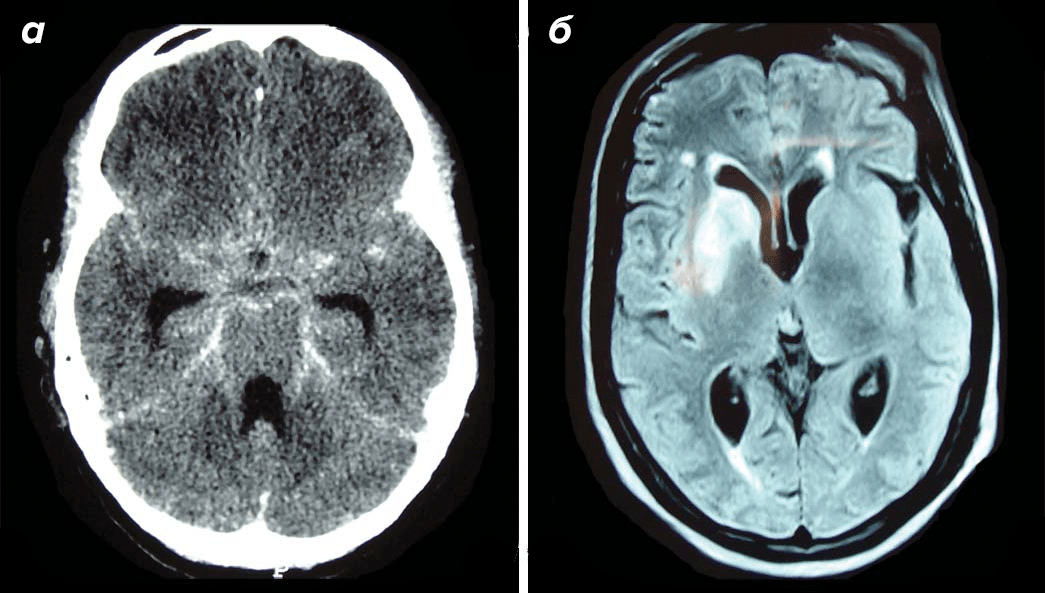
Некоторые врачи считают не совсем корректным название «туберкулезный менингит». Ведь помимо мозговых оболочек часто поражается и само вещество мозга. Поэтому правильнее называть такой менингит туберкулезным менингоэнцефалитом. Вместе с классическими патологическими изменениями в мозговых оболочках возникают еще и такие нарушения, как гидроцефалия (рис. 9а) и инфаркты мозгового вещества (рис. 9б) [18].
Рисунок 9. Поражения мозга при туберкулезном менингоэнцефалите. а — КТ 19-летнего пациента с туберкулезным менингоэнцефалитом с развившейся гидроцефалией. б — МРТ 56-летнего пациента, страдающего туберкулезным энцефалитом с инфарктом базальных ганглиев.
Сложность лечения туберкулезного менингита заключается в том, что менингеальные симптомы возникают намного позже самого заражения, поскольку болезнь развивается достаточно медленно. Из-за этого диагноз ставят поздно, и лечение в этот момент уже значительно затруднено.
Применение БЦЖ — вакцины против туберкулеза — хорошо защищает от заболевания туберкулезным менингитом. Согласно данным метаанализа, частота туберкулезного менингита в группах, вакцинированных БЦЖ, снизилась на 73%.
Вирусный менингит
Вирусный, или серозный менингит (также его иногда называют асептическим), протекает легче, чем бактериальный: у него не такая тяжелая симптоматика и более короткий период восстановления. Нередко вирусный менингит даже не требует госпитализации. Частота вирусного менингита в наших широтах — 1 на 100 тысяч человек [19], однако точное количество заболевших сложно оценить, поскольку часто люди переносят заболевание «на ногах», не прибегая к медицинской помощи и даже не зная о том, что заболели. Если заболевание протекает в легкой форме, то больной может поправиться самостоятельно через 7–10 дней. Чаще всего вирусным менингитом заболевают дети, а также люди с ослабленной иммунной системой (например, с иммунодефицитом или после химиотерапии).
Самыми распространенными вирусными возбудителями менингита являются энтеровирусы: вирус Коксаки и эховирус [20]. Второе по распространенности семейство вирусов, вызывающих воспаление мозговых оболочек, — герпесвирусы, чаще всего заражающие детей и молодых людей в развивающихся странах [21]. Вирус простого герпеса типа 1, помимо менингита вызывающий еще и генитальный герпес, является причиной так называемого рецидивного менингита, или менингита Молларета. Симптомы этой болезни схожи с классическими, однако возникают лишь на 2–5 день, а затем внезапно пропадают. Обычно у заболевших бывает около трех (иногда более) менингеальных приступов. Вирус варицелла-зостер также вызывает менингит, и, помимо него, ветрянку.
У пациентов с ВИЧ также может развиться так называемый криптококковый менингит, вызванный грибковой инфекцией Cryptococcus neoformans или же Cryptococcus gatti.
Помимо всех описанных вирусов, менингит могут вызывать также вирус гриппа, вирус лихорадки Западного Нила и вирус лимфоцитарного хориоменингита.
Для вирусного менингита характерны сезонные вспышки [20]. Например, энтеровирусы в умеренном климате чаще заражают людей летом или осенью. А вирус лихорадки Западного Нила, больше всего встречающийся в Северной Америке, активен в конце лета.
В сентябре 2018 года была зарегистрирована вспышка вирусного менингита: на Сахалине и в Сахалинской области около 50 детей попали в больницы с подозрением на серозный (вирусный) менингит. Позднее диагноз был подтвержден. Возраст пострадавших варьировал от 8 месяцев до 16 лет, а очагом заражения оказались два детских сада в Южно-Сахалинске. Вспышка на Сахалине окончилась удачно — случаев инвалидности и смерти не было.
Приблизительно в то же время случай менингита вирусной природы был обнаружен и на Урале. Болезнь зафиксировали в Тюмени и Екатеринбурге, а очаг инфекции — гимназию в Екатеринбурге, где заболел 21 ребенок, — Роспотребнадзор закрыл на карантин.
Протозойный менингит
Простейшие (или протозои)— группа эукариот, которые не относятся ни к животным, ни к растениям, ни к грибам. Протозойный менингит встречается значительно реже, чем бактериальный или вирусный, чаще всего на фоне серьезного иммунодефицита, например, при ВИЧ-инфекции [25], [26]. В остальных случаях, если иммунная система человека не ослаблена, менингит при заражении Тoxoplasma gondii не разовьется.
Как можно заразиться менингитом?
В основном менингит передается воздушно-капельным путем: если находиться рядом с больным человеком, который чихает или кашляет на вас, шансы заразиться довольно велики. В группы риска попадают люди со сниженным иммунитетом, курильщики (даже пассивные), люди, находящиеся в эндемичных по менингиту районах в местах большого скопления людей, а также люди возраста 0–5, 15–24 и старше 65 лет.
Для каждого возбудителя менингита есть свои нюансы распространения, приведенные в таблице 1.
| Возбудитель | Способ передачи инфекции |
|---|---|
| Neisseria meningitidis | воздушно-капельный |
| Streptococcus pneumoniae | воздушно-капельный, во время родов при соприкосновении кожи и слизистых ребенка с биологическими жидкостями матери |
| Haemophilus influenzae | воздушно-капельный |
| Listeria monocytogenes | фекально-оральный, во время родов при соприкосновении кожи и слизистых ребенка с биологическими жидкостями матери |
| Escherichia coli | фекально-оральный, во время родов при соприкосновении кожи и слизистых ребенка с биологическими жидкостями матери |
| Mycobacterium tuberculosis | ингаляционный/контактный, гематогенный |
| Picornaviridae | воздушно-капельный, фекально-оральный |
| Herpesviridae | воздушно-капельный, фекально-оральный, половой, во время родов при соприкосновении кожи и слизистых ребенка с биологическими жидкостями матери |
| Toxoplasma gondii | при попадании ооцист из окончательного хозяина (кошки) в промежуточного хозяина — человека |
Классическим воздушно-капельным путем передаются основные возбудители менингита Neisseria meningitidis, Streptococcus pneumoniae и Haemophilus influenzae. Все эти бактерии живут в слизистой горла человека и распространяются с брызгами слюны. Довольно часто человек, в горле которого обитает менингококк, является лишь его носителем, однако при ослаблении иммунитета эта бактерия может попасть в кровоток и проникнуть в мозг, вызвав заражение. Носительство менингококка встречается примерно в 1–10% случаев, однако при эпидемии может возрасти до 25%. Аналогична ситуация и с пневмококком — он выявляется больше чем у половины населения [27].
В некоторых случаях стрептококк и кишечная палочка передаются от матери к ребенку при родах — при соприкосновении кожи и слизистых ребенка с биологическими жидкостями матери. При этом бактерии могут вызвать заражение новорожденного менингитом.
Бактерия Listeria monocytogenes может передаваться от человека к человеку через еду, воду или предметы бытового обихода, то есть фекально-оральным способом. Одна из главных опасностей в данном случае — грязные руки. Таким же способом передается и другой возбудитель менингита, Escherichia coli.
Туберкулезный менингит передается гематогенным способом — с током крови. При первичном или вторичном туберкулезе легких бактерии попадают в кровь и, проходя через гематоэнцефалический барьер, оказываются в мозгу.
Распространение вирусов, вызывающих менингит, аналогично. Большинство из них передается при близком контакте с инфицированным человеком (воздушно-капельным путем), через слизистые глаз, рта или через воду фекально-оральным способом. Некоторые вирусы (например, герпесвирусы) могут передаваться половым путем или от матери к ребенку при рождении.
Особый способ распространения у Toxoplasma gondii. Это простейшее развивается в основном и промежуточном хозяевах. Основным хозяином являются кошки, в кишечнике которых из цист, поглощенных животным, образуются ооцисты, попадающие затем в организм человека через фекалии и вызывающие различные поражения тканей, в том числе и менингит.
Диагностика и лечение менингита
Экстренная диагностика менингита в домашних условиях
При бактериальном менингите инкубационный период инфекции составляет 2–10 дней (как правило, около 4 дней). В это время чрезвычайно важно распознать, заболел ли пациент именно менингитом, так как раннее обращение за помощью позволяет существенно снизить вероятность тяжелых осложнений и избежать летального исхода. Помимо лабораторных исследований (о них ниже), заболевшие могут самостоятельно определить основные симптомы болезни и в случае возникновения подозрения на менингит срочно обратиться за помощью.
Общие симптомы менингита похожи на симптомы при некоторых простудных заболеваниях. Они включают в себя высокую температуру, головную боль и неприятные ощущения в мышцах. Более специфическими симптомами являются рвота, иногда спутанность сознания и чувствительность к свету. При заболевании они могут появляться в любом порядке и не обязательно все. Еще более специфическими симптомами являются ригидность затылочных мышц, а также симптомы Кернига и Брудзинского. Однако важно помнить об их низкой чувствительности (всего лишь 5%! [28]): их отсутствие отнюдь не дает гарантии, что пациент не болен менингитом. Поэтому важно использовать их для подтверждения болезни, но отнюдь не для ее исключения.
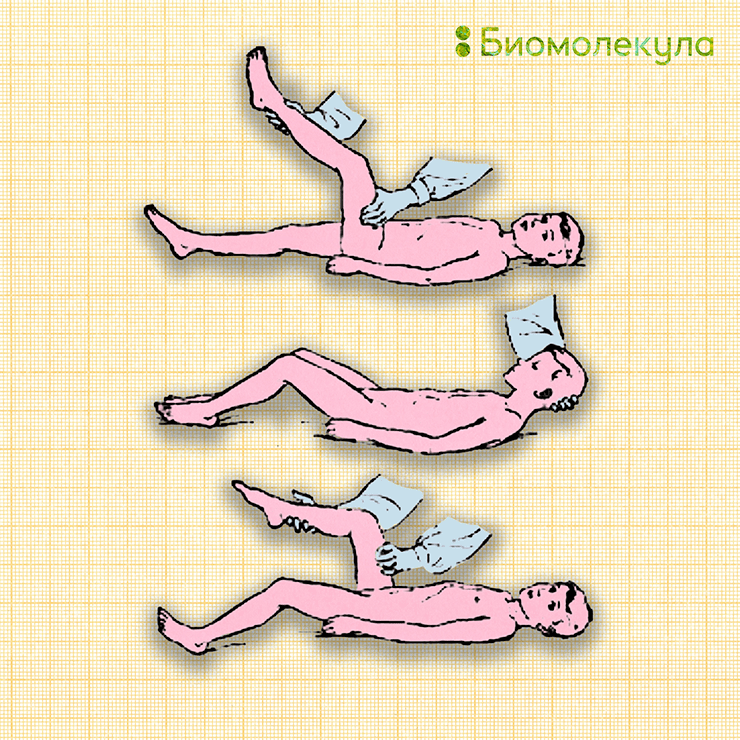
Рисунок 10. Специфические симптомы при менингите. Сверху вниз: симптом Кернига, верхний симптом Брудзинского, нижний симптом Брудзинского.
Симптом Кернига (рис. 10) заключается в том, что ногу пациента невозможно разогнуть в коленном суставе, когда она согнута в тазобедренном.
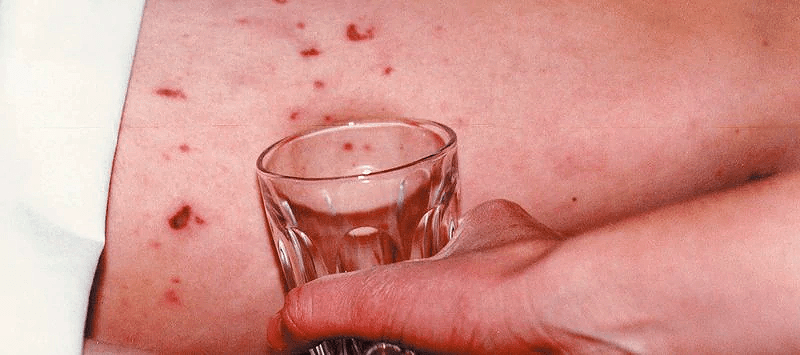
Одним из наиболее характерных признаков менингококкового (как и пневмококкового) сепсиса служит возникновение геморрагической «звездчатой» сыпи (рис. 11). Отличить опасную сыпь от менее опасных часто помогает несложный стаканный тест. Если при нажатии стенкой стакана на пораженный участок кожи сыпь не исчезает — следует насторожиться; это могут быть и петехии/пурпура (травматические, от васкулита или от дефицита/дефекта тромбоцитов), но если у пациента есть лихорадка, интоксикация, головная боль и сыпь, не пропадающая от нажатия стаканом, — срочный осмотр врача для исключения менингококцемии совершенно необходим.
Рисунок 11. Стаканный тест (glass test). Если сыпь при прикладывании стакана не пропадает — это повод подозревать менингококковый сепсис и немедленно обратиться к врачу.
Однако сыпь бывает не во всех случаях болезни (и не всегда на ранних ее стадиях). Кроме того, даже если сыпь исчезает под давлением, однозначно исключить менингит нельзя, поэтому стаканный тест не следует использовать как абсолютный инструмент для диагностики менингококкового/пневмококкового сепсиса.
Если симптомы вирусного менингита напоминают симптомы гриппа, то туберкулезный менингит довольно сложно отличить от классического бактериального. В любом случае, при любых недомоганиях со схожими с менингитом симптомами стоит немедленно обращаться в больницу, ведь счет идет на часы.
Клиническая диагностика менингита
Для подбора корректной терапии необходимы клинические лабораторные тесты, ведь симптомы могут оказаться очень неспецифическими, и по ним одним сложно будет определить, каким типом менингита страдает пациент (и менингит ли это вообще).
Однако перед тем как приступить к лабораторной клинической диагностике, полезно бывает собрать историю болезни пациента: был ли контакт с зараженными менингитом людьми, путешествовал ли он в эндемичные по менингиту районы, и каков его иммунологический статус (страдает ли от ВИЧ или других иммунодефицитов), есть ли у пациента лекарственные аллергии, использовал ли он в последнее время антибиотики и т.д. Всё это поможет врачу точнее определить, болен ли пациент менингитом, и каково его происхождение.
Чтобы правильно диагностировать и распознать менингит с помощью лабораторных тестов, ВОЗ даже разработала многостраничную инструкцию, в которой описывается каждый конкретный способ диагностики, правила проведения тестов и их возможные результаты.
После сбора анамнеза проводится лабораторная диагностика менингита. Для этого больному делают люмбальную пункцию. Это процедура, в ходе которой при местном обезболивании забирают пробу спинномозговой жидкости для дальнейшего лабораторного исследования и диагностики заболевания. Наиболее удобным местом для проведения пункции являются промежутки между III и IV и между II и III поясничными позвонками. У взрослого человека спинной мозг заканчивается на уровне II поясничного позвонка, потому вероятность повреждения спинного мозга при этой процедуре минимальна.
Образец спинномозговой жидкости изучают, обращая внимание на:
и другие показатели, необходимые для точного определения возбудителя менингита.
Диагноз «бактериальный менингит» ставят при следующих результатах исследования:
Детям младше трех месяцев с температурой неизвестной этиологии люмбальную пункцию рекомендовано делать в обязательном порядке, поскольку симптомы менингита в этом возрасте чаще всего неспецифические, а риск того, что ребенок может пострадать от этого заболевания, очень велик.
Лечение
Лечение менингита подбирают в зависимости от того, какой патоген его вызвал. В основном это, конечно, внутривенное введение антибиотиков (пенициллина, ампициллина и цефтриаксона). В России для лечения гнойного менингита в качестве антибиотиков первого ряда рекомендуется принимать бензилпенициллин, цефтриаксон или цефотаксим. Если же бактерии-возбудители оказываются устойчивы к этим антибиотикам, то добавляют хлорамфеникол (левомицетин сукцинат) или ампициллин. Решение об их использовании принимают на основе результатов лабораторных тестов. Помимо антибиотиков необходимо обеспечить больному восполнение жидкости в организме, а в случае возникновения проблем с дыханием — кислородную маску.
Для ликвидации отека мозга врачи обычно начинают терапию кортикостероидами (дексаметазоном), что позволяет снизить вероятность осложнений на слуховой аппарат и других неврологических проблем.
Вакцинация от менингита
Вакцинация против менингита должна быть комплексной, поскольку возбудителей этой болезни очень много. Основными являются менингококк, пневмококк и гемофильная палочка типа В, поэтому мы остановимся на вакцинах, которые защищают именно от этих бактерий. Однако не стоит забывать и про вирусные менингиты, которые возникают в том числе как осложнения при заболевании корью [23] и эпидемическим паротитом [22]. Профилактическая вакцинация от этих болезней также чрезвычайно важна, им посвящены отдельные статьи нашего спецпроекта. Остальные возбудители (увы!) иммунопрофилактике не поддаются.
Виды вакцин
О том, какие бывают вакцины и чем они друг от друга отличаются, рассказано в статье «Разработка вакцин: чем и как имитировать болезнь?» спецпроекта [30]. — Ред.
Белковая вакцина используется для защиты от менингококка серотипа В. Дело в том, что полисахариды капсулы бактерии этой серогруппы схожи с полисахаридами в тканях нервной системы человека, что может привести к серьезным побочным реакциям на вакцину [31]. Поэтому в состав такой вакцины входят не полисахариды, а белок оболочки бактерии (см. табл. 2).
Об основных типах иммунных клеток и их совместной работе при уничтожении возбудителей инфекции рассказано в статье «Иммунитет: борьба с чужими и своими» [32]. — Ред.
Конъюгированные вакцины от менингококка состоят из белка, соединенного с полисахаридом (опять же различных серогрупп менингококка). Такая вакцина вызывает у человека Т-клеточный и В-клеточный иммунные ответы и дальнейшее формирование иммунологической памяти, которая позволяет защитить вакцинируемого от заболевания менингитом на долгие годы (табл. 2) и, таким образом, гораздо лучше подходит для плановой вакцинации, чем полисахаридная.
Конъюгированные и белковая вакцины способствуют формированию коллективного иммунитета. Если привито большое количество людей (более 90% населения), то передача возбудителя от человека к человеку затруднена, что позволяет защитить тех людей, которым прививки противопоказаны.
| Свойство | Полисахаридная вакцина | Конъюгированная вакцина | Белковая вакцина |
|---|---|---|---|
| Т-клеточный ответ | нет | да | да |
| Иммунологическая память | нет | да | да |
| Стойкая защита | нет (защита до 3 лет) | да (5 лет и более) | да (длительность неизвестна) |
| Эффект ревакцинации* | нет | да | да |
| Коллективный иммунитет | нет | да | да |
| * Эффект ревакцинации — более интенсивный ответ организма на повторный контакт с антигеном | |||
Итак, против менингококка могут использоваться вакцины каждого из трех описанных выше типов, различающиеся в том числе и серотипами возбудителя, от которых они защищают. Так, полисахаридная четырехвалентная вакцина MPSV4 (Menomune) защищает от четырех серотипов менингококка (А, С, W-135, Y) и действует кратковременно. Menomune считается единственной вакциной, которую можно вводить взрослым пациентам старше 55 лет. Конъюгированная четырехвалентная вакцина MCV4 (Menveo или Menactra) защищает от четырех серотипов менингококка (А, С, W-135, Y) и может быть использована как для взрослых, так и для детей. Она позволяет обеспечить долговременную защиту организма. Вакцина MenB (Trumenba или Bexsero) также относится к конъюгированным вакцинам, однако вторым компонентом в ее составе является не полисахарид, а белок оболочки менингококка серотипа В — это единственная вакцина с таким спектром действия.
Против пневмококка используются полисахаридные и конъюгированные вакцины, например, полисахаридная вакцина PPSV23 (Pneumovax), защищающая от 23 серотипов и применяемая для вакцинации детей, конъюгированная вакцина PCV10 («Синфлорикс»), применяемая для вакцинации детей и защищающая от 10 серотипов, а также конъюгированная вакцина PCV13 (Prevenar), защищающая от 13 серотипов и взрослых, и детей. PCV13 и PCV10 ввиду того, что являются конъюгированными, вызывают более длительный и сильный иммунный ответ, поэтому единственное преимущество над ними PPSV23 — более широкий спектр серотипов.
Вакцины против гемофильной палочки типа В, как правило, многокомпонентны, то есть защищают не только от этого патогена, но и от некоторых других. Компонент, отвечающий за защиту от ХИБ, у них конъюгированный. Так, вакцина Hib/MenC (Menitorix) защищает также и от менингококка серотипа С, а DTaP/IPV/Hib/HepB (Infanrix hexa) — от дифтерии, столбняка, коклюша, гепатита В и полиомиелита.
Вакцинация от менингита в России
В России для защиты от пневмококка (всем детям) и гемофильной палочки В (только группам риска) предусмотрена плановая вакцинация. Обязательной же вакцинации от менингококка в Национальном календаре профилактических прививок нет, однако она предусмотрена для групп риска и по эпидемиологическим показаниям.
Согласно Национальному календарю профилактических прививок, вакцинация от пневмококка проводится всем детям трехкратно. В таблице 3 приведены все вакцины от пневмококка, доступные в России. Вакцинацию от гемофильной палочки типа В проводят детям, которые находятся в группе риска, а именно тем, кто страдает неврологическими заболеваниями или заболеваниями кишечника, детям с иммунодефицитами и детям в домах ребенка. Вакцинацию проводят четырежды: в 3, 4,5, 6 и 18 месяцев.
От менингококка в России зарегистрировано три вакцины: одна отечественная полисахаридная и две импортные конъюгированные — «Менактра» и «Менвео» (табл. 3). Бесплатную вакцинацию «Менактрой» проводят для лиц из групп риска, однако она также доступна платно для всех желающих. Жестких правил по графику вакцинации от менингококка нет. Производители зарубежных вакцин советуют прививать детей в возрасте от 2 месяцев курсом из трех прививок с перерывом в 2 месяца, а четвертую прививку проводить на втором году жизни (в 12–16 месяцев).
Для некоторых субъектов России вакцинация против менингококка доступна более широко, информацию об этом следует искать в локальных нормативных актах. Так, в Москве рассчитывать на бесплатную вакцинацию могут все дети 3–6 лет.
Противопоказания при вакцинации от менингита стандартные. Это симптомы любого острого заболевания, хроническое заболевание вне ремиссии и возникновение немедленных аллергических реакций на предыдущие введения вакцины.
| Патоген | Название вакцины | Тип вакцины | Схема вакцинации (дети) | Схема вакцинации (взрослые) |
|---|---|---|---|---|
| Пневмококк | «Синфлорикс» | 10-валентная конъюгированная | с 6 недель до 5 лет, схемы введения различаются в зависимости от возраста | не проводится |
| «Превенар 13» | 13-валентная конъюгированная | от четырех до одной дозы в зависимости от возраста; вакцинация проводится с 2 месяцев. | однократно | |
| «Пневмо 23», «Пневмовакс 23» | 23-валентная полисахаридная | первая вакцинация после 2 лет, ревакцинация каждые 5 лет | людям из группы риска — каждые 5 лет | |
| Гемофильная палочка типа В | «Акт-ХИБ» | полисахаридная конъюгированная | четырехкратно в возрасте 3, 4,5, 6 и 18 месяцев | не проводится |
| «Хиберикс» | полисахаридная конъюгированная | |||
| «Пентаксим» | конъюгированная, комбинированная с дифтерийной, столбнячной, коклюшной, полиомиелитной вакцинами | |||
| «Инфанрикс Гекса» | конъюгированная, комбинированная с дифтерийной, столбнячной, коклюшной, полиомиелитной вакцинами и вакциной против гепатита В | |||
| Менингококк | Вакцина менингококковая группы А | полисахаридная | с 1 года однократно, ревакцинация каждые 3 года | при эпидемиологической угрозе — однократно, ревакцинация каждые 3 года |
| «Менвео» | конъюгированная четырехвалентная | двукратно или четырехкратно в зависимости от возраста | однократно | |
| «Менактра» | конъюгированная четырехвалентная | двукратно с 9 месяца жизни |
Безопасность превыше всего
Вакцинация против менингита безопасна, но все же стоит помнить о редких нежелательных реакциях на прививку, не являющихся осложнениями и проходящих через некоторое время:
Полисахаридные вакцины исключительно редко вызывают даже небольшое покраснение в месте укола. Побочные эффекты на конъюгированные вакцины также возникают достаточно редко, но чуть чаще, чем на полисахаридные. Например, мышечная боль наблюдалась у 13% пациентов, вакцинированных «Менактрой», против 3% у вакцинированных полисахаридной вакциной [33].
В 2006 году несколько привитых пациентов в США пожаловались на то, что у них развился синдром Гийена—Барре — острое аутоиммунное воспаление периферических нервов. Однако проведенное в 2012 году крупное исследование показало, что развитие этого синдрома не связано с вакцинацией против менингита [34].
Взгляд в будущее
В настоящее время ВОЗ ведет широкую кампанию по борьбе с менингитом.
Во-первых, необходимо работать над взятием эпидемий под контроль и их предотвращением. ВОЗ делает упор на повышение доступности вакцин к возбудителям менингита в тех странах, где это необходимо, в первую очередь, вакцин против менингококка в странах «менингитного пояса».
Во-вторых, очень важно уделить внимание диагностике. Много ресурсов необходимо вложить в развитие более быстрых и доступных способов диагностировать менингит. Например, планируется разработать тест, который позволял бы ставить диагноз по анализу крови, а не спинномозговой жидкости. Ранняя и корректная диагностика менингита может существенно снизить смертность и предотвратить тяжелые осложнения от болезни.
В-третьих, планируется более качественный сбор статистики по заболеваемости менингитом в мире. На данный момент нет четкой картины того, что происходит во всем мире. Причем такая проблема наблюдается не только в Африке, но и в Восточной Европе, Северной и Южной Америках, Австралии. Полное видение проблемы позволит снизить заболеваемость и процент осложнений и применять корректные меры по борьбе с менингитом.
В-четвертых, ВОЗ подчеркивает необходимость усовершенствовать качество поддержки, оказываемой пациентам, которые перенесли менингит, и их семьям. Такие пациенты часто сталкиваются не только с последующими проблемами со здоровьем, но и со стигматизацией и другими социальными трудностями. Пристальное внимание к проблеме позволит облегчить жизнь тех, кого не миновала эта болезнь.
И, наконец, в-пятых, необходимо повышать вовлеченность различных государственных, благотворительных и здравоохранительных структур в проблему заболеваемости менингитом. Появление большого количества благотворительных организаций и государственных программ может внести существенный вклад в повышение качества медицинского обслуживания и реабилитации пациентов, особенно в африканских странах с эпидемиологической угрозой менингита.
Бактериальный менингит — одно из страшных заболеваний с высокой летальностью и риском инвалидизации. Размышляя над тем, необходимо ли вакцинироваться от него, всегда стоит помнить — а стоит ли страх перед прививками серьезных последствий этой коварной болезни?