Как выглядит под микроскопом феррит
Микроструктура стали
Химический состав стали и режимы ее кристаллизации и дальнейшей обработки (термообработки, обработки давлением) определяют ее структуру, а структура стали определяет ее свойства, а знание свойств необходимо при проектировании изделий из стали. Поэтому контролю или изучению микроструктуры металлов уделяется много внимания.
Идею для данной статьи мне подал Олег Олегович, читатель из г. Владимира, за что ему огромное спасибо!
Полиморфизм железа
Прежде чем говорить про структуры сталей, хочу напомнить, что из статьи про полиморфизм железа мы знаем, что в твердом состоянии у железа существуют две модификации с разной кристаллической решеткой: модификация с объёмоцентрированной кубической (ОЦК) решеткой (1392—1539 °C и медленно охлаждаем сталь, углеродистую например, с 1000°С до 800°С, структура перестраивается с ГЦК в ОЦК, а следовательно, углероду становится тесновато. Тогда часть атотмов углерода, которые уже не помещаются, прихватывают с собой по три атома железа и уходят из решетки, образуя самостоятельное соединение – цементит Fe3C. Это как в переполненном автобусе: если неудачно стоите, вас выносят с собой на ближайшей остановке.
А теперь к теме статьи – к структурам.
Структуры сталей
В сталях можем видеть следующие структуры:
Естественно, что тема эта очень обширная и ей посвящен не один учебник, а эта классификация затрагивает далеко не все возможные структуры (бейнитный феррит, вырожденный перлит и т.п.), но для общего представления, думаю, достаточно. Для более глубокого понимания и детального изучения, конечно, стоит почитать соответствующую литературу типа [1, 3], на которую я и буду ссылаться далее с приведением конкретных страниц.
Собственно, для того блог и сделан, чтобы упорядочить информацию и всегда иметь под рукой отправные точки — ссылки с указанием страниц, где можно посмотреть более подробно.
Ниже привожу таблицу с определениями и типичными изображениями микроструктур.
| Название | Определение, описание | Пример |
| Аустенит | Это твердый раствор углерода и других элементов в γ-железе [1, стр. 146]. Более сложное определение из [3, стр. 74]: «термин аустенит применяют для определения первичного твердого раствора, который образует гранецентрированное кубическое γ-железо с большинством металлов и некоторыми неметаллическими элементами». |  [3, стр. 136] Ширина кадра 800 мкм. |
| Феррит | Твердый раствор углерода и других элементов в α-железе [1, стр. 146]. Вот посложнее [3, стр. 76] : [3, стр. 141] Ширина кадра 800 мкм. | |
| Цементит | Цементит – «химическое соединение углерода с железом» (карбид железа) с формулой Fe3C [1, стр. 147-148]. | см. в ниже в структуре перлита |
| Перлит | «Эвтектоидная смесь феррита и цементита» [1, стр. 151]. «Две фазы — феррит и цементит, образуются в виде чередующихся пластинок, которые растут одновременно от границ по направлению к центру аустенитных зёрен» [3, стр. 77]. |  [3, стр. 203] Ширина кадра 160 мкм. Оптический микроскоп. |
| Сорбит | Перлит тонкого строения [1, стр. 220], т.е. пластинки феррита и цементита тоньше, чем у обычного перлита. Появляется при более высоких степенях переохлаждения, чем при образовании обычного перлита. |  [3, стр. 158]. Ширина кадра 16 мкм. Электронный микроскоп. |
| Троостит | Также феррито-цементитная смесь пластинчатого строения, но еще более тонкого строения по сравнению с сорбитом. Появляется при еще более высоких степенях переохлаждения. |  [3, стр. 160]. Ширина кадра 16 мкм. Электронный микроскоп. |
| Зернистый перлит | Феррито-цементиная смесь. Цементит находится в феррите в форме зернышек. |  [3, стр. 159] Ширина кадра 160 мкм. Оптический микроскоп. |
| Мартенсит | Продукт фазового превращения, происходящего по сдвиговому, бездиффузионному механизму [1, стр. 229]. |  [3, стр. 182] Ширина кадра 80 мкм. Оптический микроскоп. |
| Бейнит | Продукт промежуточного превращения. Имеет как признаки превращения по сдвиговому механизму, так и по диффузионному. |  Зернистый бейнит [3, стр. 167] Ширина кадра 160 мкм. Оптический микроскоп. |
Феррит
[3, стр. 141] Ширина кадра
800 мкм.
Оптический микроскоп.

Видманштедтов феррит (белый) [3, стр. 151]. Ширина кадра
800 мкм.
Оптический микроскоп.
Рис. Изменение свободной энергии модификаций железа [1, стр. 146]
Видманштедтов феррит появляется при достаточно быстром охлаждении от температуры выше А3 (см. диаграмму Fe-C), но не таком быстром, чтобы прошло бейнитное или мартенситное превращение. Что-то между. В плоскости шлифа феррит выглядит как иглы (см рис. выше).
Перлит
Образуется при медленном охлаждении сталей с содержанием углерода более 0,02% [3]. Перлит похож на слоистую смесь: чередующиеся пластины феррита и цементита (как фанера). Именно в цементит и уходит углерод при превращении железа из α в γ.
[3, стр. 156] Ширина кадра
160 мкм. Оптический микроскоп.
[3, стр. 156] Ширина кадра
160 мкм. Оптический микроскоп.
Пластинчатый перлит. Однородный по химическому составу аустенит всегда превращается в перлит пластинчатого строения [1, стр. 221]. Например, при термической обработке, когда мы нагреваем сталь от комнатной температуры до относительно высоких температур (выше Ас3), получаем гомогенный (однородный по хим. составу) аустенит, поскольку интенсивно протекают процессы диффузии: атомы растворенных химических элементов идут из мест, где их больше, в места, где их меньше. При медленном охлаждении такого аустенита получим пластинчатый перлит.
Троостит. Появляется при скоростях охлаждения чуть меньше υк (критическая скорость охлаждения по достижении которой начинается мартенситное превращение). Пластинки различимы только в электронном микроскопе, который большие увеличения по сравнению с оптическим микроскопом.
[3, стр. 159] Ширина кадра
45 мкм. Оптический микроскоп.
Все эти структуры: перлит, сорбит, троостит, зернистый перлит, — имеют одну и ту же природу. Это смеси феррита и цементита. Отличаются они лишь формой и размерами частиц цементита — пластинок или зерен.
Мартенсит
[3, стр. 184] Ширина кадра
160 мкм. Оптический микроскоп.
[3, стр. 183] Ширина кадра
160 мкм. Хорошо видны рейки мартенсита. Крупные белые участки — остаточный аустенит. Оптический микроскоп.
Мы рассмотрели, как протекает медленное превращение. Существует критическая скорость охлаждения стали, при которой (или больше нее) происходит интересная вещь: железо все равно перестраивает свою структуру, но уже не по диффузионному, а по сдвиговому механизму. Сталь резко охладили, и по законам природы вроде бы нужно при меньших температурах иметь другую кристаллическую решетку. Вот она и перестраивается, только резко, и атомы меняют свое положение целыми группами.
Представим ряды солдат (атомы Fe), среди которых стоят гражданские (атомы С).
Получается вот что: углерод остался сидеть в решетке, а превращение прошло, и решетка перестроилась. Что тогда с решеткой-то творится, если в ней места для углерода нет?
Мартенсит, согласно [Стр. 232], классифицируют на два основных типа – пластинчатый и реечный.
Бейнит
[3, стр. 167] Ширина кадра
800 мкм.
Оптический микроскоп.

[3, стр. 173] Ширина кадра
800 мкм.
Оптический микроскоп.
Структура, которая образуется по промежуточному механизму (есть следы как сдвигового превращения, так и диффузионного). Рассмотрим ту же аналогию с солдатами и гражданскими лицами. Среди гражданских (атомов C) нашлись те, кто почуял неладное и выбежал из строя (вышли из решетки по диффузионному механизму), а часть – не успели (остались в твердом растворе), солдаты же в это время перестроились по заготовленному сценарию.
Чаще всего бейнит представляет собой смесь феррита в виде реек и цементита или остатков непревращённого аустенита ( остаточного аустенита), которые окантовывают эти ферритные рейки.
Аустенит
[3, стр. 136] Хорошо видны термические двойники внутри зерна аустенита, которое даже в кадр не поместилось. Ширина кадра
160 мкм.
Оптический микроскоп

[3, стр. 183] Ширина кадра
Крупные белые участки — остаточный аустенит. Оптический микроскоп.
Аустенит в виде зерен можно увидеть только у сталей с повышенной устойчивостью аустенита (т.е. в которой помимо железа имеется еще высокое содержание легирующих элементов типа хрома и никеля): в этих сталях при быстром охлаждении превращения аустенита в феррит не происходит. У обычных углеродистых или малолегированных сталей при охлаждении мы будем получать феррит, перлит, бейнит или мартенсит в зависимости от скорости охлаждения.
Например, в стали с 18% Сr и 8%Ni быстрым охлаждениемот температур порядка 1100 ° С можно стабилизировать аустенит, который будет существовать и при комнатных температурах. Данное состояние при комнатных температурах не очень-то естественно для металла: мы ведь охладили его быстро, не дав никакого шанса атомам, сидящих в решетке (находящихся в твердом растворе) покинуть аустенит, поэтому металл находится в напряжении. Происходит деформация металла вследствие напряжений сжатия: в решетке зерен сидит углерод, который искажает решетку, а сами зерна давят друг на друга, т.е. каждое зерно подвергается сжатию. Эта деформация сжатия вызывает появление большого количества двойников [3, стр. 112]. Что такое двойники, мы уже знаем из статьи про сложности при определении размера зерна.
Все. Ура! Наконец-то закончил! Надеюсь, статья будет полезной. Если есть замечания, пишите.
Ссылки
1. Гуляев А.П. — Металловедение, М. «Металлургия», 1986, 282 с.
2.Kohlhaas R., Dünner P., Schmitz-Pranghe N. – Z. angew. Phys. 1967. 23. №3. 245-249
3. Металлография железа. Том 1. «Основы металлографии». Перев. с англ. М: «Металлургия», 1972, 240 с.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Зерна стали под световым микроскопом
Оптическая микроскопия является основным инструментом для оценки зеренной структуры сталей. Обычно структуру, которую видят в световой микроскоп, называют микроструктурой. Механические свойства любой стали сильно зависят от ее микроструктуры.
Вид зерен стали в световой микроскоп
Структура зерен железа и стали выявляется путем полирования ее поверхности до зеркального блеска, травления в кислотном растворе и осмотра под световым микроскопом (см. Структура зерна чистого железа).
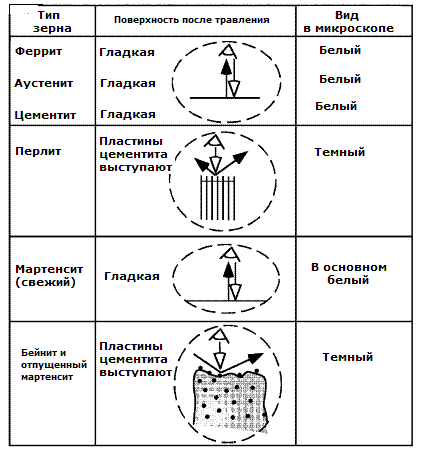
В результате травления с полированной поверхности удаляются атомы, а скорость этого удаления зависит от ориентации кристалла зерна и типа зерна, например, феррита или аустенита. Контрастность данного зерна под микроскопом зависит от степени гладкости его поверхности после травления.
Как показано на рисунке 1 зерна, которые являются одной и той же фазой, такой как феррит, аустенит, цементит, будут травиться равномерно по всей поверхности. Поэтому после травления исходная зеркальная поверхность останется гладкой внутри каждого отдельного зерна.
Рисунок 1 – Вид различных типов зерен в стали в световой микроскоп
Как работает световой микроскоп
Световой микроскоп использует для формирования своих изображений отраженный свет. Луч света направляется сверху вниз на поверхность стали (светлые стрелки на рисунке 1). Изображение формируется фотопленкой (фотопластинкой, цифровым устройством) или глазом от света, который отражается вдоль того же направления (черные стрелки).
Для гладкой поверхности очень большая доля света, пришедшего на образец, отразиться обратно и создаст яркое (белое) изображение. Поэтому однофазные зерна феррита, аустенита и цементита будут выглядеть белыми. Поскольку они выглядят белыми их часто невозможно различить под микроскопом без дополнительной информации.
Структура перлита под световым микроскопом
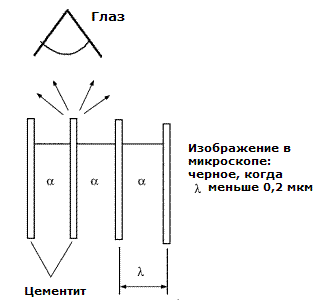
Рассмотрим теперь перлит. Обычными травителями, которые применяют для сталей, являются нитал (азотная кислота в спирте) и пикрал (пикриловая кислота в спирте). Эти травители травят ферритные пластины перлита значительно быстрее, чем цементитные пластины. Поэтому после травления цементитные пластины выступают из ферритных пластин. Цементитные пластины являются очень тонкими, и они хорошо рассеивают падающий на них свет (рисунок 2). Это приводит к формированию темносерого изображения. По этой причине перлит выглядит под световым микроскопом в оттенках от серого до черного.
Рисунок 2 – Отражение света от травленой поверхности перлита
Однако так бывает не всегда. Если расстояние между цементитными пластинами достаточно велико, они выглядят как темные линии с белыми ферритными пластинами между ними. Оптический микроскоп може «видеть» только расстояния до приблизительно 0,2 мкм при максимальном увеличении около 1000х. Поэтому, когда межпластиночное расстояние в перлите становиться менее 0,2 мкм, то оптический микроскоп показывает перлитные зерна в виде темносерых пестрых изображений, как это показано на рисунке 3.
Межпластиночное расстояние в перлите
Расстояние между цементитными пластинами в перлите зависит от того, на сколько быстро образец охлаждался из аустенитной области через температуру А1 – чем быстрее охлаждение, тем меньше это расстояние. Обычно, чтобы достичь такое охлаждение образец просто вынимают из печи и позволяют ему охладиться на воздухе.
Скорость охлаждения, понятно, зависит от размеров образца. Даже для довольно больших образцов охлаждение на воздухе дает межпластиночное расстояние меньше чем 0,2 мкм. Поэтому перлит в образцах, которые охлаждались на воздухе, почти всегда выглядят так как на рисунке 3.
Рисунок 3 – Фотография микроструктуры структуры перлита: травитель – пикрал, увеличение при съемке — 500х
Пикраловый травитель, который применялся для образца на рисунке 3, растворяет феррит более однородно при изменении ориентации кристаллов зерен, чем это делает ниталовый травитель. Поэтому пикрал дает более однородный серый цвет для каждого зерна и он является предпочтительным травителем для перлита.
Диаграмма состояния «железо — углерод»
Содержание
Компоненты в системе «железо-углерод»
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит:
Железо
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри. Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв=250 МПа, предел текучести – σт=120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ=50 %, а относительное сужение – ψ=80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Фазы в системе «железо-углерод»
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
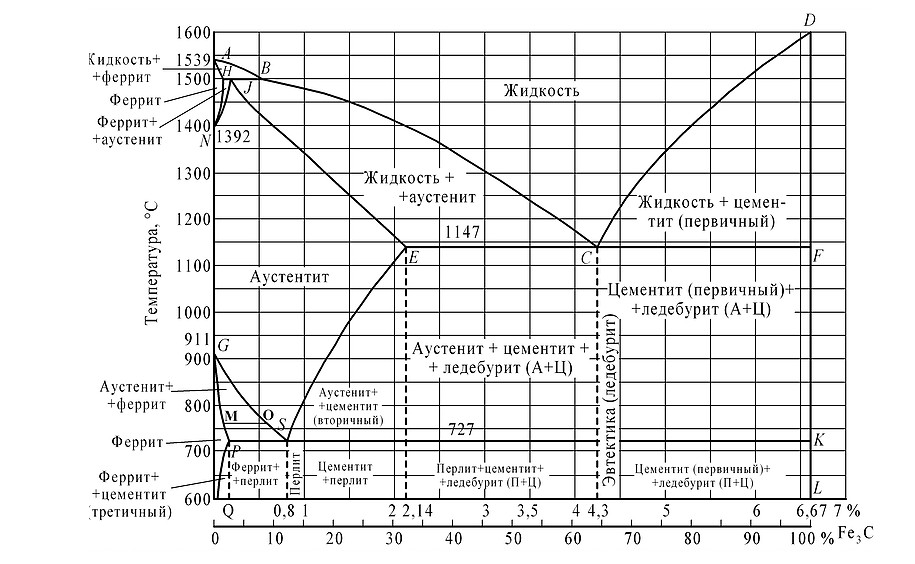
Диаграмма состояния железо-углерод
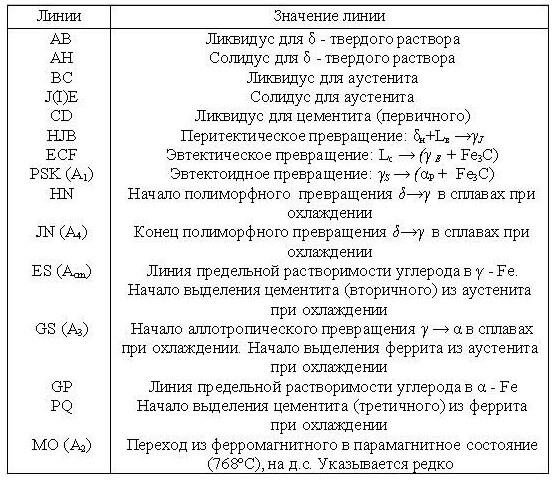
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Другие структурные составляющие в системе «железо-углерод»
Перлит
Ледебурит в сталях
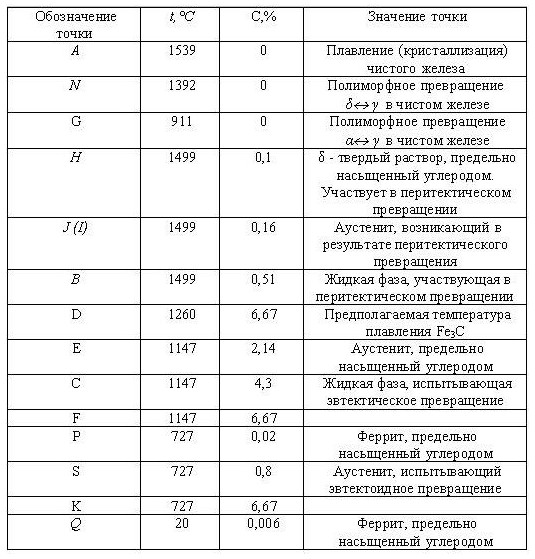
Узловые критические точки диаграммы состояния системы железо-углерод
Узловые критические точки диаграммы железо-углерод
Значение линий диаграммы состояния системы железо-углерод
Значения линий на диаграмме железо-углерод
Всякая диаграмма состояния показывает условия равновесного сосуществования фаз во взятой системе компонентов.
Полное физико-химическое равновесие между фазами может быть достигнуто только в специальных лабораторных условиях, а на практике некоторым приближением к этому состоянию может быть случай чрезвычайно медленного охлаждения или нагрева сплава с весьма длительными выдержками во времени при любых искомых температурах.
Цементит — структура, свойства, виды
Диаграмма состояния железо-углерод (цементит) — это графическое отображение фазового состава и структуры сплавов в зависимости от концентрации углерода и температуры
Содержание
Описание
Концентрация углерода в цементите — 6,67% по массе — предельная для железоуглеродистых сплавов. Цементит — метастабильная фаза; образование стабильной фазы — графита во многих случаях затруднено. Цементит имеет орторомбическую кристаллическую решётку, очень твёрд и хрупок, слабо магнитен до 210 °C.
В зависимости от условий кристаллизации и последующей обработки цементит может иметь различную форму — равноосных зёрен, сетки по границам зёрен, пластин, а также видманштеттову структуру.
Цементит в разных количествах, в зависимости от концентрации, присутствует в железоуглеродистых сплавах уже при малых содержаниях углерода. Формируется в процессе кристаллизации из расплава чугуна. В сталях выделяется при охлаждении аустенита или при нагреве мартенсита. Цементит является фазовой и структурной составляющей железоуглеродистых сплавов, составной частью ледебурита, перлита, сорбита и троостита. Цементит — представитель так называемых фаз внедрения, соединений переходных металлов с лёгкими металлоидами. В фазах внедрения велики доля как ковалентной, так и металлической связи.
Твёрдость по Бринеллю больше 800 кг/мм2.
Первичный цементит кристаллизуется из жидкого сплава
Вторичный цементит — из аустенита
Третичный цементит — из феррита
Компоненты в системе «железо-углерод»
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит:
Железо
Железо – d-переходный металл серебристо-светлого цвета. Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3. Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри. Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв=250 МПа, предел текучести – σт=120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ=50 %, а относительное сужение – ψ=80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Химические свойства
Серый, относительно твёрдый, термически устойчивый. Не реагирует с водой, щелочами, гидратом аммиака.
Температура плавления цементита
Согласно данным Гуляева А.П. температура плавления цементита — около 1600°.
Первичный цементит
Вторичный цементит
Вторичный цементит выделяется из аустенита — γ-твёрдого раствора. При охаждении выделение происходит по линии ES (диаграмма Fe-C). Форма вторичного цементита: цементитная сетка, цементит по границам зёрен.
Третичный цементит
Третичный цементит выделяется из феррита. Форма третичного цементита: пластинки и прожилки, а также выделения в виде иголок в ферритном зерне. При более быстром охлаждении часть углерода остаётся в твёрдом растворе; выделение третичного цементита подавляется.
Другие формы существования цементита (по Хоу): цементит перлита, цементит ледебурита, цементит Стеда, зернистый цементит, специальные карбиды.
Автор обзора: Корниенко А.Э. (ИЦМ)
См. также Железоуглеродистые сплавы, Диаграмма состояния системы железо-цементит.
Фазы в системе «железо-углерод»
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 80 — 130 НВ, временное сопротивление – σв=300 МПа) и пластичен (относительное удлинение — δ=50 %), магнитен до 768° С.
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо — цементит и железо — графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе — С) — графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура — содержание углерода. Диаграмма состояния системы железо — углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран. Особое место среди них занимают работы Д.К. Чернова. Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
Диаграмма состояния железо-углерод
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус — по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % — к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии GS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) — как Аr1.
Другие структурные составляющие в системе «железо-углерод»
Кроме компонентов и фаз в системе сплавов «железо-углерод» присутствуют другие структурные составляющие — перлит и ледебурит
Перлит
Перлит — эвтектоид, механическая смесь феррита и цементита, полученная в результате распада аустенита при охлаждении сплавов ниже 727° С. При медленном охлаждении перлит присутствует во всех сплавах с концентрацией углерода от 0,02 до 6,67%. Под микроскопом перлит может выглядеть либо как пластины, либо как зерна — зернистый перлит. Его вид, также как и механические свойства, зависит от скорости охлаждения сплава и вида его термической обработки
Ледебурит в сталях
Ледебурит — эвтектика, механическая смесь аустенита и цементита, выделяющаяся из жидкости при охлаждении сплавов ниже 1147° С. Принципиальное отличие эвтектикой составляющей от эвтектоидной заключается в том, что первая выделяется из жидкости, а вторая из твердого раствора, в случае железоуглеродистых сплавов — из аустенита. Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Узловые критические точки диаграммы состояния системы железо-углерод
Значения линий на диаграмме железо-углерод
Всякая диаграмма состояния показывает условия равновесного сосуществования фаз во взятой системе компонентов.
Полное физико-химическое равновесие между фазами может быть достигнуто только в специальных лабораторных условиях, а на практике некоторым приближением к этому состоянию может быть случай чрезвычайно медленного охлаждения или нагрева сплава с весьма длительными выдержками во времени при любых искомых температурах.